
酶免疫测定(enzyme immunoassay)可分为均相(homogenous)和非均相(heterogenous)两种类型。在均相EIA中可不需进行游离的和结合的标记物的分离而直接测定标记物。例如在某种条件下,抗原抗体反应后形成的酶标记抗原抗体复合物中的酶失去其对底物作用的活力,因而测出的酶活力直接反映游离的酶标记物。均相EIA在临床检验中较少应用。非均相EIA需先进行游离的和结合的标记物的分离。自从Engvall和Perlman(1971)首次报道建立酶联免疫吸附试验(Enzyme-Linked ImmunosorbentAssays, ELISA)以来,由于ELISA具有快速、敏感、简便、易于标准化等优点,使其得到迅速的发展和广泛应用 。尽管早期的ELISA由于特异性不够高而妨碍了其在实际中应用的步伐,但随着方法的不断改进、材料的不断更新,尤其是采用基因工程方法制备包被抗原,采用针对某一抗原表位的单克隆抗体进行阻断ELISA试验,都大大提高了ELISA的特异性,加之电脑化程度极高的ELISA检测仪的使用,使ELISA更为简便实用和标准化,从而使其成为最广泛应用的检测方法之一。
ELISA的基础是抗原或抗体的固相化及抗原或抗体的酶标记。结合在固相载体表面的抗原或抗体仍保持其免疫学活性,酶标记的抗原或抗体既保留其免疫学活性,又保留酶的活性。在测定时,受检标本(测定其中的抗体或抗原)与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与液体中的其他物质分开。再加入酶标记的抗原或抗体,也通过反应而结合在固相载体上。此时固相上的酶量与标本中受检物质的量呈一定的比例。加入酶反应的底物后,底物被酶催化成为有色产物,产物的量与标本中受检物质的量直接相关,故可根据呈色的深浅进行定性或定量分析。由于酶的催化效率很高,间接地放大了免疫反应的结果,使测定方法达到很高的敏感度。
ELISA可用于测定抗原,也可用于测定抗体。在这种测定方法中有三个必要的试剂:(1)固相的抗原或抗体,即"免疫吸附剂"(immunosorbent);(2)酶标记的抗原或抗体,称为“酶联物”、“结合物”(conjugate);(3)酶反应的底物。根据试剂的来源和标本的情况以及检测的具体条件,可设计出各种不同类型的检测方法。
(一) 基本原理 ELISA方法的基本原理是酶分子与抗体或抗抗体分子共价结合,此种结合不会改变抗体的免疫学特性,也不影响酶的生物学活性。此种酶标记抗体可与吸附在固相载体上的抗原或抗体发生特异性结合。滴加底物溶液后,底物可在酶作用下使其所含的供氢体由无色的还原型变成有色的氧化型,出现颜色反应。因此,可通过底物的颜色反应来判定有无相应的免疫反应,颜色反应的深浅与标本中相应抗体或抗原的量呈正比。此种显色反应可通过ELISA检测仪进行定量测定,这样就将酶化学反应的敏感性和抗原抗体反应的特异性结合起来,使ELISA方法成为一种既特异又敏感的检测方法。
(二) 用于标记的酶 用于标记抗体或抗抗体的酶须具有下列特性:有高度的活性和敏感性;在室温下稳定;反应产物易于显现;能商品化生产。目前应用较多的有辣根过氧化物酶(HRP)、碱性磷酸酶、葡萄糖氧化酶等,其中以HRP应用最广。
1.辣根过氧化物酶(HRP) 过氧化物酶广泛分布于植物中,辣根中含量最高,从辣根中提取的称辣根过氧化物酶(HRP),是由无色酶蛋白和深棕色的铁卟啉构成的一种糖蛋白(含糖量18%),分子量约40 000,约由300个氨基酸组成,等电点为pH 3-9,催化反应的最适pH值因供氢体不同而稍有差异,一般多在pH 5左右。此酶溶于水和50%饱和度以下的硫酸铵溶液。酶蛋白和辅基的最大吸收光谱分别为275nm和403nm。
酶的纯度以RZ表示:RZ=OD403/OD275
纯酶的RZ多在3.0以上,最高为3.4。RZ在0.6以下的酶制品为粗酶,非酶蛋白约占 75%,不能用于标记。RZ在2.5以上者方可用于标记。HRP的作用底物为过氧化氢,催化反应时的供氢体有几种:(1)邻苯二胺(OPD),产物为橙色,可溶性,敏感性高,最大吸收值在490nm,可用肉眼观察判别,容易被浓硫酸终止反应,颜色可在数小时内不改变,是目前国内ELISA中最常用的一种;(2)联大茴香胺(OD),产物为橘黄色,最大吸收值在400nm,颜色较稳定;(3)5-氨基水杨酸(5-AS):产物为深棕色,最大吸收值在449nm,部分溶解,敏感性较差;(4)邻联甲苯胺(OT)产物为蓝色,最大吸收值在630nm,部分溶解,不稳定,不耐酸,但反应快,颜色明显。
2.碱性磷酸酶 系从小牛肠粘膜和大肠杆菌中提取,由多个同功酶组成。它们的底物种类很多,常用者为硝基苯磷酸盐,廉价无毒性。酶解产物呈黄色,可溶,最大吸收值在400nm。酶的活性以在pH10反应系统中,37℃1分钟水解1μg磷酸苯二钠为一个单位。
1.标记方法 良好的酶结合物取决于两个条件:即高效价的抗体和高活性的酶。抗体的活性和纯度对制备标记抗体至关重要,因为特异性免疫反应随抗体活性和纯度的增加而增强。在酶标记过程中,抗体的活性有所降低,故需要纯度高、效价高及抗原亲和力强的抗体球蛋白,最好使用亲和层析提纯的抗体,可提高敏感性,而且可稀释使用,减少非特异性吸附。
酶与抗体交联,常用戊二醛法和过碘酸盐氧化法。郭春祥建立的HRP标记抗体的改良过碘酸钠法简单易行,标记效果好,特别适用于实验室的小批量制备。其标记程序为:将5μg HRP溶于0.5ml蒸馏水中,加入新鲜配制的0.06 mol/L的过碘酸钠(NaIO4)水溶液0.5ml,混匀置4℃冰箱30分钟 , 取出加入0.16mol/L的乙二醇水溶液0.5ml,室温放置30分钟后加入含5(g纯化抗体的水溶液1ml,混匀并装透析袋,以0.05mol/L、pH9.5的碳酸盐缓冲液于4℃冰箱中慢慢搅拌透析6小时(或过夜)使之结合,然后吸出,加硼氢化钠(NaBH4)溶液( 5(g/ml)0.2ml,置4℃冰箱2小时,将上述结合物混合液加入等体积饱和硫酸铵溶液,置4℃冰箱30分钟后离心,将所得沉淀物溶于少许0.02mol/L、pH7.4PBS中,并对之透析过夜(4℃),次日离心除去不溶物,即得到酶标抗体,用0.02mol/L、pH7.4PBS稀至5ml,进行测定后,冷冻干燥或低温保存。
2.酶标抗体标记效果测定:测定内容包括酶和抗体活性、结合物中酶含量和IgG含量、酶与IgG摩尔比值以及结合率。
(1) 酶与抗体的活性 常用琼脂扩散或免疫电泳法,使抗原与抗体形成沉淀线,经PBS漂洗1天,再以蒸馏水浸泡1小时,将琼脂凝胶片浸于酶底物溶液中着色,如果出现应有的颜色反应,再用生理盐水浸泡,颜色仍然不褪,表示结合物既有酶的活性,也有抗体活性。良好的结合物在显色后,琼扩滴度应在1:16以上。另一个测定方法是用系列稀释的酶标抗体直接以ELISA方法进行方阵滴定,此法不仅可以测定标记效果,还可以确定酶标抗体的使用浓度。
(2) 结合物的定量测定 一般是对结合物中的酶和IgG进行定量测定。常用紫外分光光度计于403nm和280nm进行测定,然后按下列公式计算:
酶量(mg/ml)=OD403×0.42
IgG量(mg/ml)=(OD280-OD403×0.4)×0.94×0.62
对于过碘酸钠氧化法制备的标记抗体量,按下列公式计算:
IgG量(mg/ml)=(OD280-OD403×0.34)×0.62
已知酶量和IgG量后,即可计算出标记抗体的摩尔(mol)比值。
HRP/IgG摩尔比值=HRP(mg/ml)/IgG(mg/ml)×4
结合物中酶总量=HRP(mg/ml)×结合物溶液量
结合物产率=结合物中酶总量/标记时加入的酶量×100%
用于ELISA的结合物的酶量为400(g/ml时效果一般,为500(g/ml时效果较好,达 1000(g/ml时效果最好。mol.比值由于结合物中含的IgG并不完全可靠,所以不能作为主要参数。一般认为mol.比值为0.7时效果一般,1.0时效果较好,1.5-2.0时最好。酶结合率为 7%时效果一般,为9%-10%较好,达30%以上时最好。
根据ELISA所用的固相载体而区分为三大类型:一是采用聚苯乙烯微量板为载体的ELISA,即我们通常所指的ELISA(微量板ELISA);另一类是用硝酸纤维膜为载体的ELISA,称为斑点ELISA(Dot-ELISA);再一类是采用疏水性聚脂布作为载体的ELISA,称为布ELISA(C-ELISA)。在微量板ELISA中,又根据其性质不同分为间接ELISA、双抗体夹心ELISA、双夹心ELISA、竞争ELISA、阻断ELISA及抗体捕捉ELISA。
1.间接ELISA 本法主要用于检测抗体。以鸭病毒性肝炎(DVH)抗体的ELISA为例,间接ELISA的操作程序如下。
(1) 材料
① 包被液、洗涤液、保温液、底物液、终止液;
② DVH包被抗原、酶标抗抗体、阴性及阳性DVH参考血清;待检鸭血清;
③ ELISA检测仪、加样器、聚苯乙烯微量板。
(2) 方法步骤
① 加抗原包被 → 4℃过夜,洗涤三次、抛干
② 加待检血清 → 37℃ 2小时,洗涤三次、抛干
③ 加酶标抗体 → 37℃ 2小时,洗涤三次、抛干
④ 加底物液 → 37℃ 30分钟,加终止液
⑤ 用ELISA检测仪测定OD值,并计算出P/N比值。
(3) 结果判定 已知阳性血清与已知阴性血清的比值(P/N)≥2.1,而且已知阳性血清的OD值≥0.4;在上述条件成立的情况下,如果待检血清与已知阴性血清的比值(P/N)≥2.1,而且待检血清的OD值≥0.4,则判为阳性,否则判为阴性。
2.双抗体夹心ELISA 本法主要用于检测大分子抗原。现以检测鸡传染性法氏囊病病毒(IBDV)的双夹心抗体ELISA为例介绍本法的操作程序。
① 加抗体包被 → 4℃过夜,洗涤三次、抛干
② 加待检抗原 → 37℃ 30分钟,洗涤三次、抛干
③ 加酶标抗体 → 37℃ 30分钟,洗涤三次、抛干
④ 加底物液 → 37℃ 15分钟,加终止液
⑤ 用ELISA检测仪测定OD值。
3.双夹心ELISA 此法与双抗体夹心ELISA的主要区别在于:它是采用酶标抗抗体检查多种大分子抗原,它不仅不必标记每一种抗体,还可提高试验的敏感性。此法的基本程序为:
① 加抗体(Ab-1)包被 → 4℃过夜,洗涤三次、抛干
② 加待检抗原(Ag) → 37℃ 60分钟,洗涤三次、抛干
③ 加用非同种动物生产的特异性抗体(Ab-2)→ 37℃ 60分钟,洗涤三次、抛干
④ 加入酶标抗Ab-2抗体(AB-3)→ 37℃ 60分钟,洗涤三次、抛干
⑤ 加底物液 → 37℃ 20分钟,加终止液
⑥ 用ELISA检测仪测定OD值。
4.竞争ELISA 此法主要用于测定小分子抗原及半抗原,其原理类似于放射免疫测定。其基本程序为:
① 抗体包被 → 4℃过夜,洗涤三次、抛干
② 加入待检抗原及一定量的酶标抗原(对照孔仅加酶标抗原)→ 37℃ 60分钟,洗涤三次、抛干
③ 加底物液 → 37℃ 20分钟,加终止液
④ 用ELISA检测仪测定OD值。
被结合的酶标抗原的量由酶催化底物反应产生有色产物的量来确定,如果待检溶液中抗原越多,被结合的标记抗原的量就越少,有色产物就减少,这样根据有色产物的变化就可求出未知抗原的量。此法的优点在于快速、特异性高、且可用于小分子抗原及半抗原的检测;其主要不足在于每种抗原都要进行酶标记,而且因为抗原的结构不同,还需应用不同的结合方法。此外,试验中应用酶标抗原的量较多。
5.阻断ELISA 本法主要用于检测型特异性抗体。该方法现已成为猪传染性胃肠炎(TGE)、猪伪狂犬病(PR)及猪胸膜肺炎(AP)的主要检测方法。下面以AP2型抗体的阻断ELISA检测法为例介绍其操作程序:
① 100μl AP2型工作量抗原包被 → 4℃过夜,洗涤三次、抛干
② 用200μl阻断缓冲液进行封闭 → 37℃ 60分钟,洗涤三次、抛干
③ 加工作量1:4稀释被检猪血清100μl → 37℃ 60分钟,洗涤三次、抛干
④ 加100μl工作量兔抗AP2型血清 → 37℃ 30分钟,洗涤三次、抛干
⑤ 加100μl工作量猪抗兔IgG-HRP → 37℃ 60分钟,洗涤三次、抛干
⑥ 加100μl OPD底物液 → 37℃ 20分钟,加终止液
⑦ 用ELISA检测仪测定OD值。
本试验同时设标准阴、阳性血清对照、兔抗AP2型阳性对照、空白对照。
6.抗体捕捉ELISA 本法主要用于检测IgM抗体。由于IgM抗体出现于感染早期,所以检测出IgM,则可作为某种疾病的早期诊断。抗体捕捉ELISA根据所用标记方式不同可分为标记抗原、标记抗体、标记抗抗体捕捉ELISA等几种,其中以标记抗原捕捉ELISA比较有代表性,该方法的主要程序为:
① 用抗u链(抗IgM重链)抗体包被→37℃ 60分钟后置4℃过夜,洗涤三次、抛干
② 加待检血清 → 37℃ 2小时,洗涤三次、抛干
③ 加酶标抗原 → 37℃ 60分钟,洗涤三次、抛干
④ 加底物液 → 37℃ 20分钟,加终止液
⑤ 用ELISA检测仪测定OD值。
7.斑点ELISA(Dot-ELISA) 与常规的微量板ELISA比较,Dot-ELISA具有简便、节省抗原等优点,而且结果可长期保存;但其也有不足,主要是在结果判定上比较主观,特异性不够高等。该方法的主要操作程序为:
(1) 载体膜的预处理及抗原包被 取硝酸纤维素膜用蒸馏水浸泡后,稍加干燥进行压圈。将阴性、阳性抗原及被检测抗原适度稀释后加入圈中,置37℃使硝酸纤维素膜彻底干燥。每张7cm×2.3cm的膜一般可点加40-53个样品,每个压圈可加抗原液1-20μl。
(2) 封闭 将硝酸纤维素膜置于封闭液中,37℃感作15-30分钟。封闭液多采用含有正常动物血清、pH7.2或pH7.4的PBS。
(3) 加被检血清 可直接在抗原圈上加,也可剪下抗原圈、置于微量板孔中,再加入一定量适度稀释的待检血清,37℃反应一定时间,用洗涤液洗三次,每次1-3分钟。洗涤液一般为一定浓度的PBS-Tween溶液。
(4) 加酶标抗体,37℃反应一定时间后,用洗涤液洗三次。
(5) 显色 加入新鲜配制的底物液,37℃反应一定时间后,去掉底物液,加蒸馏水洗涤终止反应。
(6) 结果判定 以阳性、阴险血清作为对照,膜片中央出现深棕红色斑点者为阳性反应,否则为阴性反应。
8.布ELISA(C-ELISA) C-ELISA(Cloth-ELISA)是加拿大学者Blais, B. W.等于1989年建立的一种新型免疫检测技术。该方法是以疏水性聚脂布(Hydrophobic Polyester Cloth)即涤纶布为固相载体,这种大孔径的的疏水布具有吸附样品量大,可为免疫反应提供较大的表面积,提高反应的敏感性,且容易洗涤,不需特殊仪器等优点。其基本原理与Dot-ELISA类似,只是载体不同。以对布氏杆菌抗原的检测为例,C-ELISA的主要程序为:
(1) 首先把抗布氏杆菌的血清包被(吸附)在聚脂布上,并经洗涤及封闭;
(2) 加被检样品并于室温下感作30分钟,然后洗5次;
(3) 加酶标记的抗布氏杆菌抗体,于室温下感作30分钟,然后洗涤5次;
(4) 加入底物液显色;
(5) 测定OD值。
1 双抗体夹心法测抗原
双抗体夹心法是检测抗原最常用的方法,操作步骤如下:
1) 将特异性抗体与固相载体联结,形成固相抗体。洗涤除去未结合的抗体及杂质。
2) 加受检标本,保温反应。标本中的抗原与固相抗体结合,形成固相抗原抗体复合物。洗涤除去其他未结合物质。
3) 加酶标抗体,保温反应。固相免疫复合物上的抗原与酶标抗体结合。彻底洗涤未结合的酶标抗体。此时固相载体上带有的酶量与标本中受检抗原的量相关。
4) 加底物显色。固相上的酶催化底物成为有色产物。通过比色,测知标本中抗原的量。
在临床检验中,此法适用于检验各种蛋白质等大分子抗原,例如HBsAg、HBeAg、AFP、hCG等。只要获得针对受检抗原的异性抗体,就可用于包被固相载体和制备酶结合物而建立此法。如抗体的来源为抗血清,包被和酶标用的抗体最好分别取自不同种属的动物。如应用单克隆抗体,一般选择两个针对抗原上不同决定簇的单抗,分别用于包被固相载体和制备酶结合物。这种双位点夹心法具有很高的特异性,而且可以将受检标本和酶标抗体一起保温反应,作一步法检测。
在一步法测定中,当标本中受检抗原的含量很高时,过量抗原分别和固相抗体及酶标抗体结合,而不再形成"夹心复合物"。类同于沉淀反应中抗原过剩的后带现象,此时反应后显色的吸光值(位于抗原过剩带上)与标准曲线(位于抗体过剩带上)某一抗原浓度的吸光值相同,如按常法测读,所得结果将低于实际的含量,这种现象被称为钩状效应(hook effect),因为标准曲线到达高峰后呈钩状弯落。钩状效应严重时,反应甚至可不显色而出现假阴性结果。因此在使用一步法试剂测定标本中含量可异常增高的物质(例如血清中HBsAg、AFP和尿液hCG等)时,应注意可测范围的最高值。用高亲和力的单克隆抗体制备此类试剂可削弱钩状效应。
假使在被测分子的不同位点上含有多个相同的决定簇,例如HBsAg的a决定簇,也可用针对此决定的同一单抗分别包被固相和制备酶结合物。但在HBsAg的检测中应注意亚型问题,HBsAg有adr、adw、ayr、ayw4个亚型,显然每种亚型均有相同的a决定簇的反应性,这也是用单抗作夹心法应注意的问题。
双抗体夹心法测抗原的另一注意点是类风湿因子(RF)的干扰。RF是一种自身抗体,多为IgM型,能和多种动物IgG的Fc段结合。用作双抗体夹心法检测的血清标本中如含有RF,它可充当抗原成份,同时与固相抗体和酶标抗体结合,表现出假阳性反应。采用F(ab')或Fab片段作酶结合物的试剂,由于去除了Fc段,从而可消除RF的干扰。双抗体夹心法ELISA试剂是否受RF的影响,已被列为这类试剂的一项考核指标(参见6.2)。
双抗体夹心法适用于测定二价或二价以上的大分子抗原,但不适用于测定半抗原及小分子单价抗原,因其不能形成两位点夹心。
2 双抗原夹心法测抗体
反应模式与双抗体夹心法类似。用特异性抗原进行包被和制备酶结合物,以检测相应的抗体。与间接法测抗体的不同之处为以酶标抗原代替酶标抗抗体。此法中受检标本不需稀释,可直接用于测定,因此其敏感度相对高于间接法。乙肝标志物中抗HBs的检测常采用本法。本法关键在于酶标抗原的制备,应根据抗原结构的不同,寻找合适的标记方法。
3 间接法测抗体(我公司分装TORCH及传染病试剂盒大多采用本法)
间接法是检测抗体常用的方法。其原理为利用酶标记的抗抗体(抗人免疫球蛋白抗体)以检测与固相抗原结合的受检抗体,故称为间接法。操作步骤如下:
1)将特异性抗原与固相载体联结,形成固相抗原。洗涤除去未结合的抗原及杂质。
2)加稀释的受检血清,保温反应。血清中的特异抗体与固相抗原结合,形成固相抗原抗体复合物。经洗涤后,固相载体上只留下特异性抗体,血清中的其他成份在洗涤过程中被洗去。
3)加酶标抗抗体。可用酶标抗人Ig以检测总抗体,但一般多用酶标抗人IgG检测IgG抗体。固相免疫复合物中的抗体与酶标抗体抗体结合,从而间接地标记上酶。洗涤后,固相载体上的酶量与标本中受检抗体的量正相关。
4)加底物显色
本法主要用于对病原体抗体的检测而进行传染病的诊断。间接法的优点是只要变换包被抗原就可利用同一酶标抗抗体建立检测相应抗体的方法。
间接法成功的关键在于抗原的纯度。虽然有时用粗提抗原包被也能取得实际有效的结果,但应尽可能予以纯化,以提高试验的特异性。特别应注意除去能与一般健康人血清发生反应的杂质,例如以E.Coli为工程酶的重组抗原,如其中含有E.Coli成份,很可能与受过E.Coli感染者血清中的抗E.Coli抗体发生反应。抗原中也不能含有与酶标抗人Ig反应的物质,例如来自人血浆或人体组织的抗原,如不将其中的Ig去除,试验中也发生假阳性反应。另外如抗原中含有无关蛋白,也会因竟争吸附而影响包被效果。
间接法中另一种干扰因素为正常血清中所含的高浓度的非特异性抗体。病人血清中受检的特异性IgG只占总IgG中的一小部分。IgG的吸附性很强,非特异IgG可直接吸附到固相载体上,有时也可吸附到包被抗原的表面。因此在间接法中,抗原包被后一般用无关蛋白质(例如牛血清蛋白)再包被一次,以封闭(blocking)固相上的空余间隙。另外,在检测过程中标本须先行稀释(1:40~1:200),以避免过高的阴性本底影响结果的判断。
4 竞争法测抗体
当抗原材料中的干扰物质不易除去,或不易得到足够的纯化抗原时,可用此法检测特异性抗体。其原理为标本中的抗体和一定量的酶标抗体竞争与固相抗原结合。标本中抗体量越多,结合在固相上的酶标抗体愈少,因此阳性反应呈色浅于阴性反应。如抗原为高纯度的,可直接包被固相。如抗原中会有干扰物质,直接包被不易成功,可采用捕获包被法,即先包被与固相抗原相应的抗体,然后加入抗原,形成固相抗原。洗涤除去抗原中的杂质,然后再加标本和酶标抗体进行竞争结合反应。竞争法测抗体有多种模式,可将标本和酶标抗体与固相抗原竞争结合,抗HBc ELISA一般采用此法。另一种模式为将标本与抗原一起加入到固相抗体中进行竞争结合,洗涤后再加入酶标抗体,与结合在固相上的抗原反应。抗HBe的检测一般采用此法。
5 竞争法测抗原
小分子抗原或半抗原因缺乏可作夹心法的两个以上的位点,因此不能用双抗体夹心法进行测定,可以采用竞争法模式。其原理是标本中的抗原和一定量的酶标抗原竞争与固相抗体结合。标本中抗原量含量愈多,结合在固相上的酶标抗原愈少,最后的显色也愈浅。小分子激素、药物等ELISA测定多用此法。
6 捕获包被法测抗体(经典方法)
IgM抗体的检测用于传染病的早期诊断中。间接法ELISA一般仅适用于检测总抗体或IgG抗体。如用抗原包被的间接法直接测定IgM抗体,因标本中一般同时存在较高浓度的IgG抗体,后者将竞争结合固相抗原而使一部份IgM抗体不能结合到固相上。因此如用抗人IgM作为二抗,间接测定IgM抗体,必须先将标本用A蛋白或抗IgG抗体处理,以除去IgG的干扰。在临床检验中测定抗体IgM时多采用捕获包被法。先用抗人IgM抗体包被固相,以捕获血清标本中的IgM(其中包括针对抗原的特异性IgM抗体和非特异性的IgM)。然后加入抗原,此抗原仅与特异性IgM相结合。继而加酶标记针对抗原的特异性抗体。再与底物作用,呈色即与标本中的IgM成正相关。此法常用于病毒性感染的早期诊断。
类风湿因子(RF)同样能干扰捕获包被法测定IgM抗体,导致假阳性反应。因此中和IgG的间接法近来颇受青睐,用这类试剂检测抗CMV IgGM和抗弓形虫IgM抗体已获成功。
7 ABS-ELISA法
ABS为亲和素(avidin)生物素(biotin)系统(system)的略语。亲和素是一种糖蛋白,分子量60000,每个分子由4个能和生物素结合的亚基组成。生物素为小分子化合物,分子量244。用化学方法制成的衍生物素-羟基琥珀酰亚胺酯可与蛋白质和糖等多种类型的大小分子形成生物素标记产物,标记方法颇为简便。生物素与亲和素的结合具有很强的特异性,其亲和力较抗原抗体反应大得多,两者一经结合就极为稳定。由于一个亲和素可与4个生物素分子结合,因此如把ABS与ELISA法可分为酶标记亲和素-生物素(LAB)法和桥联亲和素-生物素(ABC)法两种类型。两者均以生物素标记的抗体(或抗原)代替原ELISA系统中的酶标抗体(抗原)。在LAB中,固相生物素先与不标记的亲和素反应,然后再加酶标记的生物素以进一步提高敏感度。在早期,亲和素从蛋清中提取,这种卵亲和素为碱性糖蛋白,与聚苯乙烯载体的吸附性很强,用于ELISA中可使本底增高。从链霉菌中提取的链霉亲和素则无此缺点,在ELISA应用中有替代前者的趋势。由于ABS-ELISA较普通ELISA多用了两种试剂,增加了操作步骤,在临床检验中ABS-ELISA应用不多。
科研项目中检测微量的成分如细胞因子常采用本法。
已包被抗原或抗体的固相载体在低温(2~8℃)干燥的条件下一般可保存6个月以上。有些不完整的试盒,仅供应包被用抗原或抗体,检测人员需自行包被。以下简述固相载体和包被过程。
1 固相载体
固相载体在ELISA测定过程中作为吸附剂和容器,不参与化学反应。可作ELISA中载体的材料很多,最常用的是聚苯乙烯。聚苯乙烯具有较强的吸附蛋白质的性能,抗体或蛋白质抗原吸附其上后仍保留原来的免疫学活性,加之它的价格低廉,所以被普遍采用。聚苯乙烯为塑料,可制成各种形式。
ELISA载体的形状主要有三种:微量滴定板、小珠和小试管。以微量滴定板最为常用,专用于EILSA的产品称为ELISA板,国际上标准的微量滴定板为8×12的96孔式。为便于作少量标本的检测,有制成8联孔条或12联孔条的,放入座架后,大小与标准ELISA板相同。ELISA板的特点是可以同时进行大量标本的检测,并可在特制的比色计上迅速读出结果。现在已有多种自动化仪器用于微量滴定板型的ELISA检测,包括加样、洗涤、保温、比色等步骤,对操作的标准化极为有利。聚苯乙烯经射线照射后,其吸附性能特别是对免疫球蛋白的吸附性能增加,应用于双抗体夹心法可使固相上抗体量增多,但用于间接法测抗体时空白值较大。
良好的ELISA板应该是吸附性能好,空白值低,孔底透明度高,各板之间、同一板各孔之间、同一板各孔之间性能相近。聚苯乙烯ELISA板由于原料的不同和制作工艺的差别,各种产品的质量差异很大,因此,每一批号的ELISA板在使用前须事先检查其性能。常用的检查方法为:以一定浓度的人IgG(一般为10ng/ml)包被ELISA板各孔,洗涤后每孔内加入适当稀释度的酶标抗人IgG抗体,保温后洗涤,加底物显色,终止酶反应后,分别测每孔溶液的吸光度。控制反应条件,使各孔读数在吸光度0.8左右。计算全部读数的平均值。所有单个读数与全部读数的均数之差,应小于10%。
与聚苯乙烯类似的塑料是聚氯乙烯。作为ELISA固相载体,聚氯乙烯的特点为质软板薄,可剪割,价廉,但光洁度不如聚苯乙烯板,孔底亦不如聚苯乙烯平整。聚氯乙烯对蛋白质的吸附性能比聚苯乙烯高,但空白值也略高。
为比较不同固相在某一ELISA测定中的优劣,可应用如下的试验:用其他免疫学测定方法选出一个典型的阳性标本和阴性标本,将它们进行一系列稀释后,在不同的固相载体上按预定的ELISA操作步骤进行测定,然后比较结果。在哪一种载体上阳性结果与阴性结果差别最大,这种载体就是这一ELISA测定项目的最合适的固相载体。
在ELISA中,用作固相载体的小珠一般为直径0.6cm的圆珠,表面经磨砂处理后吸附面积大大增加。ELISA板孔的吸附面积约为200mm2,小珠均为1000mm2,将近ELISA板孔的5倍。吸附面积的增大即意味着固相抗原或抗体量的增加。再者,球型小珠的表面弧度更有利于吸附的抗原决定簇或抗体结合位点的暴露面处于最佳反应状态,因此珠式ELISA的反应往往更为灵敏。小珠的另一特点是更易于使洗涤彻底,使用特殊的洗涤器,使小珠在洗涤过程中滚动淋洗,其洗涤效果远较板孔的浸泡式为好。但由于磨砂工艺的难度较大,小珠的均一性较差。
小试管作为固相载体也有较大的吸附表面,而且标本的反应量也相应增加。板式及珠式ELISA的标本量一般为00-200ul,而小试管可根据需要加大反应体积,标本反应量的增加有助于试验敏感性的提高。小试管还可以当作比色杯,最后直接放入分光光度计中比色。
也有应用聚苯乙烯胶乳或其他材料制成的微粒作为ELISA固相载体的。其优点是表面积极大,反应在悬液中进行,其速率与液相反应近似。以含铁的磁性微粒作为ELISA固相载体,反应后用磁铁的吸引进行分离,洗涤方便,试剂盒一般均配以特殊仪器。
2 包被的方式
将抗原或抗体固定在过程称为包被(coating)。换言之,包被即是抗原或抗体结合到固相载体表面的过程。蛋白质与聚苯乙烯固相载体是通过物理吸附结合的,靠的是蛋白质分子结构上的疏水基团与固相载体表面的疏水基团间的作用力。这种物理吸附是非特异性的,受蛋白质的分子量、等电点、浓度等的影响。载体对不同蛋白质的吸附能力是不相同的,大分子蛋白质较小分子蛋白质通常含有更多的疏水基团,故更易吸附到固相载体表面。IgG对聚苯乙烯等固相具有较强的吸附力,其联结多发生在Fc段上,抗体结合点暴露于外,因此抗体的包被一般均采用直接吸附法。蛋白质抗原大多也可采用与抗体相似的方法包被。当抗原决定簇存在于或邻近于疏水区域时,抗原与固相载体的直接吸附可使抗原决定簇不能充分暴露,在这种情况下,直接包被效果不佳,可以采用间接的捕获包被法,即先将针对该抗原的特异抗体作预包被,其后通过抗原抗体反应使抗原固相化。此间接结合在固相上的抗原远离载体表面,其抗原决定簇也得以充分暴露。间接包被的抗原经固相抗体的亲和层析作用,包被在固相上的抗原纯度大大提高,因此含杂质较多的抗原也可采用捕获包被法,试验的特异性、敏感性均由此得以改善,重复性亦佳。间接包被的另一优点是抗原用量少,仅为直接包被的1/10乃至于/100。不易吸附在聚苯乙烯载体上的非蛋白质抗原可采用特殊的包被方式。例如,在检测抗DNA抗体时,需用DNA作为包被抗原,而普遍的固相载体一般不能直接与核酸结合。可将聚苯乙烯板先经紫外线照射(例如30W紫外灯,75cm照射12小时),以增加其吸附性能。固相载体先用碱性蛋白质,如聚赖氨酸、鱼精蛋白等作预包被,也可提高核酸的结合力。也可用亲和素生物素系
统作间接包被,即用亲和素先包被载体,然后加入生物素化的DNA,这种包被方法均匀、牢固,已扩大应用于各种抗原物质的定量测定。
脂类物质无法与固相载体结合,可将其在有机溶剂(例如乙醇)中溶解后加入ELISA板孔中,开盖置冰箱过夜或冷风吹干,待酒精挥发后,让脂质自然干固在固相表面。抗心磷脂抗体的ELISA试剂一般采用这种包被方式。
3 包被用抗原
用于包被固相载体的抗原按其来源不同可分为天然抗原、重组抗原和合成多肽抗原三大类。天然抗原可取自动物组织、微生物培养物等,须经提取纯化才能作包被用。如HBsAg可以从携带者的血清中提取,一般的细菌和病毒抗原可以从其培养物中提取,蛋白成份抗原可从富含此抗原的材料中提取等(例如AFP从脐带血或胎肝中提取)。重组抗原是抗原基因在质粒体中表达的蛋白质抗原,多以大肠杆菌或酵母菌为质粒体。重组抗原的优点是除工程菌成份外,其他杂质少,而且无传染性,但纯化技术难度较大。以大肠杆菌为质粒体的重组抗原如不能充分除大肠杆菌成份,用于ELISA,在反应中可出现假阳性,因不少受检者受大肠杆菌感染而在血清中存在抗大肠杆菌抗体。重组抗原的另一特点是能用基因工程制备某些无法从天然材料中分离的抗原物质。例如丙型肝炎病毒(HCV)尚不能培养成功,而且丙肝病人血清中HCV抗原含量极微。目前检测抗HCV ELISA中所用包被抗原大多为根据HCV的基因克隆表达而制备的重组抗原。在传染病诊断中,不少重组抗原如HBsAg、HBeAg和HIV抗原等均在ELISA中取得应用。合成多肽抗原是根据蛋白质抗原分子的某一抗原决定簇的氨基酸序列人工合成的多肽片段。多肽抗原一般只含有一个抗原决定簇,纯度高,特异性也高,但由于分子量太小,往往难于直接吸附于固相上。多肽抗原的包被一般需先使其与无关蛋白质如牛血清白蛋白质(BSA)等偶联,借助于偶联物与固相载体的吸附,间接地结合到固相载体表面。应用多肽抗原的另一注意点为他仅能检测与其相应的抗体。一种蛋白质抗原往往含有多个不同的能引起抗体产生的决定簇,因此在受检血清中的其他抗体就不能与该多肽抗原发生反应。另外,某些微生物发生变异时往往发生抗原结构变化,在这种情况下,用个别多肽抗原进行包被可引起其他抗体的漏检。
4 包被用抗体
包被固相载体的抗体应具有高亲和力和高特异性,可取材于抗血清或含单克隆抗体的腹水或培养液。如免疫用抗原中含有杂质(即便是极微量的),在抗血清中将出现杂抗体,必须除去(可用吸收法)后才能用于ELISA,以保证试验的特异性。抗血清不能直接用于包被,应先提取IgG,通常采用硫酸铵盐析和Sephadex凝胶过滤法。一般经硫酸铵盐析粗提的IgG已可用于包被,高度纯化的IgG性质不稳定。如需用高亲和力的抗体包被以提高试验的敏感性,则可采用亲和层析法以除去抗血清中含量较多的非特异性IgG。腹水中单抗的浓度较高,特异性亦较强,因此不需要作吸收和亲和层析处理,一般可将腹水作适当稀释后直接包被,必要时也可用纯化的IgG。应用单抗包被时应注意,一种单抗仅针对一种抗原决定簇,在某些情况下,用多种单抗混合包被,可取得更好的效果。
5 包被的条件
包被用抗原或抗体的浓度,包被的温度和时间,包被液的pH等应根据试验的特点和材料的性质而选定。抗体和蛋白质抗原一般采用pH9.6的碳酸盐缓冲液作为稀释液,也有用pH7.2的磷酸盐缓冲液及pH7~8的Tris-HCL缓冲液作为稀释液的。通常在ELISA板孔中加入包被液后,在4-8℃冰箱中放置过夜,37℃中保温2小时被认为具有同等的包被效果。包被的最适当浓度随载体和包被物的性质可有很大的变化,每批材料需通过实验与酶结合物的浓度协调选定。一般蛋白质的包被浓度为100ng/ml-20ug/ml。
6 封闭
封闭(blocking)是继包被之后用高浓度的无关蛋白质溶液再包被的过程。抗原或抗体包被时所用的浓度较低,吸收后固相载体表面尚有未被占据的空隙,封闭就是让大量不相关的蛋白质充填这些空隙,从而排斥在ELISA其后的步骤中干扰物质的再吸附。封闭的手续与包被相类似。最常用的封闭剂是0.05%-0.5%的牛血清白蛋白,也有用10%的小牛血清或1%明胶作为封闭剂的。脱脂奶粉也是一种良好的封闭剂,其最大的特点是价廉,可以高浓度使用(5%)。高质量的速溶食用低脂奶粉即可直接当作封闭剂使用,但由于奶粉的成份复杂,而且封闭后的载体不易长期保存,因此在试剂盒的制备中较少应用。
封闭是否必要,取决于ELISA的模式及具体的实验条件。并非所有的ELISA固相均需封闭,封闭不当反而会使阴性本底增高。一般说来,双抗体夹心法,只要酶标记物是高活性的,操作时洗涤彻底,不经封闭也可得到满意的结果。特别是用单抗腹水直接包被时,因其中大量非抗体蛋白在包被时同样也吸附在固相表面,业已起到了类似封闭剂的作用。但在间接法测定中,封闭一般是不可少的。包被好的ELISA板干燥后放入密封袋或锡袋中,在低温可保存数月。
结合物即酶标记的抗体(或抗原),是ELISA中最关键的试剂。良好的结合物应该是既保有酶的催化活性,也保持了抗体(或抗原)的免疫活性。结合物中酶与抗体(或抗原)之间有恰当的分子比例,在结合试剂中应尽量不含有或少含有游离的(未结合的)酶或游离的抗体(或抗原)。此外,结合物尚要有良好的稳定性。
1酶
用于ELISA的酶应符合以下要求:纯度高,催化反应的转化率高,专一性强,性质稳定,来源丰富,价格不贵,制备成酶结合物后仍继续保留它的活性部分和催化能力。最好在受检标本中不存在相同的酶。另外,它的相应底物易于制备和保存,价格低廉,有色产物易于测定等。
在ELISA中,常用的酶为辣根过氧化物酶(horseradish peroxidase, HRP)和碱性磷酸酶(alkaline phosohatase, AP)。在少数商品ELISA试剂中,应用的酶尚有葡萄糖氧化酶、β-D-半乳糖苷酶和脲酶等。国产ELISA试剂一般都用HRP制备结合物。HRP是一种糖蛋白,含糖量约为18%,分子量为44000,是一种复合酶,由主酶(酶蛋白)和辅基(亚铁血红素)结合而成,是一种卟啉蛋白质。主酶无色糖蛋白在275nm波长处有最高吸收峰,辅基是深棕色的含铁卟啉环,在403nm波长处有最高吸收峰。HRP的纯度用RZ(Reinheit Zahl,德文,意为纯度数)表示,是403nm的吸光度与280nm吸光度之比,高纯度的HRP的RZ≥?.0。
HRP除符合上述的ELISA中标记酶的要求外,更有价格低廉和性质较稳定的特点。值得注意的是,在选用酶制剂时,除其纯度RZ外,更应注意酶的活力。高纯度的酶如保存不当,活力也会降低。酶制剂的活力以所含的酶活力单位表示,可用对底物作用后生成产物量的测定进行试验。
国外很多ELISA试剂采用碱性磷酸酶(AP)作为标记酶。常用的AP有两个来源,分别从大肠杆菌和小牛肠膜中提取。不同来源的酶生化特性特性略不相同,从大肠杆菌中提取的AP分子量为80000,酶作用的最适合pH为8.0;用小牛肠膜中提取的AP分子量为100000,最适pH为9.6。在ELISA中,AP系统的敏感度一般高于HRP系统,空白值也较低,但AP价格昂贵,制备结合物所得率也较HRP低。
2 抗原和抗体
制备结合物时所用抗体一般 均为纯度较高的IgG,以免在与酶联结时其他杂蛋白的干扰。最好用亲和层析纯的抗体,这样全部酶结合物均具有特异的免疫活性,可以在高稀释度进行反应,实验结果本底浅淡。如用F(ab')2进行标记,则更可避免标本中RF的干扰。在ELISA中用酶标抗原的模式不多,总的要求是抗原必须是高纯度的。
3 结合物的制备
酶标记抗体的制备方法主要有两种,即戊二醛交联法和过碘酸盐氧化法。
(1)戊二醛交联法:戊二醛是一种双功能团试剂,它可以使酶与蛋白质的氨基通过它而联结。碱性磷酸一般用此法进行标记。交联方法一步法、两步法两种。在一步法中戊二醛直接加入酶与抗体的混合物中,反应后即得酶标记抗体。
ELISA中常用的酶一般都用此法交联。它具有操作简便、有效(结合率达60%-70%)和重复性好等优点。缺点是交联反应是随机的,酶与抗体交联时分子间的比例不严格,结合物的大小也不均一,酶与酶,抗体与抗体之间也有可能交联,影响效果。诹讲椒ㄖ校?br> 先将酶与戊二醛作用,透析除去多余的戊二醛后,再与抗体作用而形成酶标抗体。也可先将抗体与戊二醛作用,再与酶联结。两步法的产物中绝大部分的酶与蛋白质是以1:1的比例结合的,较一步法的酶结合物更有助于本底的改善以提高敏感度,但其偶联的有效率较一步法低。
(2)过碘酸盐氧化法:本法只适用于含糖量较高的酶。辣根过氧化物酶的标记常用此法。反应时,过碘酸钠将HRP分子表面的多糖氧化为醛基很活泼,可与蛋白质上的氨基形成Schiff氏碱而结合。酶标记物按克分子比例联结,其最佳比例为:酶/抗体=1-2/1。此法简便有效,一般认为是HRP最可取的标记方法,但也有人认为所有试剂较为强烈,各批实验结果不易重演。
按以上方法制备的酶结合物一般都混有未结合物的酶和抗体。理论上,结合物中混有的游离酶一般不影响ELISA中最后的酶活性测定,因经过彻底洗涤,游离酶可被除去,并不影响最终的显色。但游离的抗体则不同,它会与酶标抗体竞争相应的固相抗原,从而减少了结合到固相上的酶标抗体的量。因此制备的酶结合物应予纯化,去除游离的酶和抗体后用于检测,效果更好。纯化的方法很多,分离大分子化合物的方法均可应用。硫酸铵盐析法最为简便,但效果并不理想,因为此法只能去除留在上清中的游离酶,但相当数量的游离抗体仍与酶结合物一起沉淀而不能分开。用离子交换层析或分子筛分离更为可取,高效液相层析法可将制备的结合物清晰地分成三个部分:游离酶、游离抗体和纯结合物而取得最佳的分离效果,但费用较贵。
结合物制得后,在用作ELISA试剂前尚需确定其适当的工作浓度。使用过浓的结合物,既不经济,又可使本底增高;结合物的浓度过低,则又影响检测的敏感性。所以必须对结合物的浓度予以选择。最适的工作浓度就是指结合物稀释至这一浓度时,能维护一个低的本底,并获得测定的最佳灵敏度,达到最合适的测定条件和测定费用的节省。就酶标抗体本身而言,它的有效工作浓度是指与其相应抗原包被的载体作试验时,能得到阳性反应的最高稀释度。例如某一HRP:抗人IgG制剂标明的工作浓度为1:5000,表示该制剂经1:5000稀释后,在与人IgG包被的固相作ELISA试验时,将发生阳性反应。但在用于具体的ELISA检测中,酶标抗体的最适工作浓度受到固相载体的性质、包被抗原或抗体的纯度以及整个检测系统如标本、反应温度和时间等的影响,因此必须在实际测定条件下进行"滴配"选择能达到高敏感度的最大稀释度作为试剂盒中的工作浓度。
4 结合物的保存
酶标抗体中的酶和抗体均为生物活性物质,保存不当,极易失活。高浓度的结合物较为稳定,冰冻干燥后可在普通冰箱中保存一年左右,但冻干过程中引起活力的减低,而且使用时需经复溶,颇为不便。结合物溶液中加入等体积的甘油可在低温冰箱或普通冰箱的冰格中较长时间保存。早期的ELISA试剂盒中的结合物一般均按以上两种形式供应,配以稀释液(见3.2.5)临用时按标明的稀释度稀释成工作液。现在较先进的ELISA试剂盒均已用合适的缓冲液配成工作液,使用时不需再行稀释,在4-8℃保存期可达6个月。由于蛋白质浓度较低,结合物易失活,需加入蛋白保护剂。另外再加入抗生素(例如庆大霉素)和防腐剂(HRP结合物加硫柳泵,AP结合物可加叠氮钠),以防止细菌生长。
5 结合物的稀释液
用于稀释高浓度的结合物以配成工作液。为避免结合物在反应中直接吸附在固相载体上,在稀释缓冲液中常加入高浓度的无关蛋白质(例如1%牛血清白蛋白),通过竞争以抑制结合物的吸附。一般还加入具有抑制蛋白质吸附于塑料表面的非离子型表面活性剂,如吐温20,0.05%的浓度较为适宜。在间接测定抗体时,血清标本需稀释后进行测定,也可应用这种稀释液。
1 HRP的底物
HRP催化过氧化物的氧化反应,最具代表性的过氧化物为H2O2,其反应式如下:
DH2+ H2O2 D+ H2O
上式中,DH2为供氧体,H2O2为受氢体。在ELISA中,DH2一般为无色化合物,经酶作用后成为有色的产物,以便作比色测定。常用的供氢体有邻苯二胺(O-phenylenediamine,OPD)、四甲基联苯胺(3,3',5,5'-tetramethylbenzidine,TMB)和ABTS[2,2'-azino-di-(3-ethylbenziazobine sulfonate-6)]。
OPD氧化后的产物呈橙红色,用酸终止酶反应后,在492nm处有最高吸收峰,灵敏度高,比色方便,是HRP结合物最常用的底物。OPD本身难溶于水,OPD•2HCL为水溶性。曾有报道OPD有致异变性,操作时应予注意。OPD见光易变质,与过氧化氢混合成底物应用液后更不稳定,须现配置现用。在试剂盒中,OPD和H2O2一般分成二组分,OPD可制成一定量的粉剂或片剂形式,片剂中含有发泡助溶剂,使用更为方便。过氧化氢则配入底物缓冲液中,有制成易保存的浓缩液,使用时用蒸馏水稀释。先进的ELISA试剂盒中则直接配成含保护剂的工作浓度为0.02% H2O2的应用液,只需加入OPD后即可作为底物应用液。
TMB经HRP作用后共产物显蓝色,目视对比鲜明。TMB性质较稳定,可配成溶液试剂,只需与H2O2溶液混和即成应用液,可直接作底物使用。另外,TMB又有无致癌性等优点,因此在ELISA中应用日趋广泛。酶反应用HCL或H2SO4终止后,TMB产物由蓝色呈黄色,可在比色计中定量,最适吸收波长为405nm。
ABTS虽不如OPD和TMB敏感,但空白值极低,也为一些试剂盒所采用。
另一种HRP的底物为3-(4-羟基)苯丙酸[3-(4-hydroxy)phenly propionic acid,HPPA],经HRP作用后,产物显荧光,可用荧光光度计测量。用于ELISA的优点为可加宽定量测定的线性范围。
HRP对氢受体的专一性很高,仅作用于H2O2、小分醇的过氧化物和尿素过氧化物(urea peroxide)。H2O2应用最多,但尿素过氧化物为固体,作为试剂较H2O2方便、稳定。试剂盒供应尿素过氧化物片剂,用蒸馏水溶解后,在底物缓冲液中密闭、低温(2~8℃)可稳定1年。
2 AP的底物
AP为磷酸酯酶,一般采用对硝基苯磷酸酯(p-nitrophenyl phosphate,p-NPP)作为底物,可制成片剂,使用方便。产物为黄色的对硝基酚,在405nm波长处有吸收峰。用NaOH终止酶反应后,黄色可稳定一时间。AP也有发荧光底物(磷酸4-甲基伞酮),可用于ELISA作荧光测定,敏感度较高于用显色底物的比色法。
洗涤液
在板式ELISA中,常用的稀释液为含0.05%吐温20磷酸缓冲盐水。
酶反应终止液
常用的HRP反应终止液为硫酸,其浓度按加量及比色液的最终体积而异,在板式ELISA中一般采用2mol/L。
阳性对照品和阴性对照品
阳性对照品(positive control)和阴性对照品(negative control)是检验试验有效性的控制品,同时也作为判断结果的对照,因此对照品,特别是阳性对照品的基本组成应尽量与检测标本的组成相一致。以人血清为标本的测定,对照品最好也为人血清,因为正常人血清在各种ELISA模式中可产生不同程度的本底。由于大量正常人血甭较难得到,国外试剂盒中的对照品多以复钙人血浆(recalcified human plasma)为原料,即在血浆中加入钙离子,使其中的纤维蛋白质凝固,除去凝块后所得的液体,其组成与血清相似。阴性对照品须先行检测,确定其中不含待测物质。例如HBsAg检测的阴性对照品中不可含HBsAg,最好抗HBs也是阴性。阳性对照品多以含蛋白保护剂的缓冲液为基质,其中加入一定量的待检物质,此量最好在试剂说明书中标明。加入的量应与试剂的敏感度相称,在测定中得到的吸光值与受检标本吸光值比较,可对标本中受检物质的量有一个粗略的估计。国外检测HBsAg的ELISA试剂盒检测敏感度约为0.5ng/ml,阳性对照品中含量约为10ng/ml。在对照品中一般加入抗生素和防腐剂,以利保存。
参考标准品
定量测定的ELISA试剂盒(例如甲胎蛋白质癌胚抗原测定等)应含有制作标准曲线用的参考标准品,应包括覆盖可检测范围的4-5个浓度,一般均配入含蛋白保护剂及防腐剂的缓冲液中。
方法一 用于检测未知抗原的双抗体夹心法:
1. 包被:用0.05M PH9.牰碳酸盐包被缓冲液将抗体稀释至蛋白质含量为1~10μg/ml。在每个聚苯乙烯板的反应孔中加0.1ml,4℃ 过夜。次日,弃去孔内溶液,用洗涤缓冲液洗3次,每次3分钟。(简称洗涤,下同)。
2. 加样:加一定稀释的待检样品0.1ml于上述已包被之反应孔中,置37℃ 孵育1小时。然后洗涤。(同时做空白孔,阴性对照孔及阳性对照孔)。
3. 加酶标抗体:于各反应孔中,加入新鲜稀释的酶标抗体(经滴定后的稀释度)0.1ml。37℃ 孵育0.5~1小时,洗涤。
4. 加底物液显色:于各反应孔中加入临时配制的TMB底物溶液0.1ml,37℃ 10~30分钟。
5. 终止反应:于各反应孔中加入2M硫酸0.05ml。
6. 结果判定:可于白色背景上,直接用肉眼观察结果:反应孔内颜色越深,阳性程度越强,阴性反应为无色或极浅,依据所呈颜色的深浅,以“+”、“-”号表示。也可测OD值:在ELISA检测仪上,于450nm(若以ABTS显色,则410nm)处,以空白对照孔调零后测各孔OD值,若大于规定的阴性对照OD值的2.1倍,即为阳性。
方法二 用于检测未知抗体的间接法:
用包被缓冲液将已知抗原稀释至1~10μg/ml,
每孔加0.1ml,4℃过夜。次日洗涤3次。
↓
加一定稀释的待检样品(未知抗体)0.1ml于上述已包被之反应孔
中,置37℃孵育1小时,洗涤。(同时做空白、阴性及阳性孔对照)
↓
于反应孔中,加入新鲜稀释的酶标第二抗体(抗抗体)0.1ml,
37℃孵育30-60分钟,洗涤,最后一遍用DDW洗涤。
↓
其余步骤同“双抗体夹心法”的4、5、6。
试剂器材
1. 试剂
(1) 包被缓冲液(PH9.6 0.05M碳酸盐缓冲液):
NaHCO3 1.59克
NaHCO3 2.93克
加蒸馏水至1000ml
(2) 洗涤缓冲液(PH7.4 PBS):0.15M
KH2PO4 0.2克
Na2HPO4•12H2O 2.9克
NaCl 8.0克
KCl 0.2克
Tween-20 0.05% 0.5ml
加蒸馏水至1000ml
(3) 稀释液:
牛血清白蛋白(BSA) 0.1克
加洗涤缓冲液至100ml
或以羊血清、兔血清等血清与洗涤液配成5~10%使用。
(4) 终止液(2M H2SO4):
?? 蒸馏水178.3ml,逐滴加入浓硫酸(98%)21.7ml。
(5) 底物缓冲液(PH5.0磷酸棗柠檬酸):
0.2M Na2HPO4(28.4克/L) 25.7ml
0.1M 柠檬酸(19.2克/L) 24.3ml
加蒸馏水50ml。
(6) TMB(四甲基联苯胺)使用液:
TMB(10mg/5ml无水乙醇) 0.5ml
底物缓冲液(PH5.5) 10ml
0.75%H2O2 32μl
(7) ABTS使用液:
ABTS 0.5mg
底物缓冲液(PH5.5) 1ml
3%H2O2 2μl
(8) 抗原、抗体和酶标记抗体。
(9) 正常人血清和阳性对照血清。
2. 器材:
(1) 聚苯乙烯塑料板(简称酶标板)40孔或96孔,ELISA检测仪,50μl及100μl加样器,塑料滴头,小毛巾,洗涤瓶。
(2) 小烧杯、玻璃棒、试管、吸管和量筒等。
(3) 4℃冰箱,37℃孵育箱。
注意事项
1. 正式试验时,应分别以阳性对照与阴性对照控制试验条件,待检样品应作一式二份,以保证实验结果的准确性。有时本底较高,说明有非特异性反应,可采用羊血清、兔血清或BSA等封闭。
2. 在ELISA中,进行各项实验条件的选择是很重要的,其中包括:
(1) 固相载体的选择:许多物质可作为固相载体,如聚氯乙烯、聚苯乙烯、聚丙酰胺和纤维素等。其形式可以是凹孔平板、试管、珠粒等。目前常用的是40孔聚苯乙烯凹孔板。不管何种载体,在使用前均可进行筛选:用等量抗原包被,在同一实验条件下进行反应,观察其显色反应是否均一性,据此判明其吸附性能是否良好。
(2) 包被抗体(或抗原)的选择:将抗体(或抗原)吸附在固相载体表面时,要求纯度要好,吸附时一般要求PH在9.0~9.6之间。吸附温度,时间及其蛋白量也有一定影响,一般多采用4℃ 18~24小时。蛋白质包被的最适浓度需进行滴定:即用不同的蛋白质浓度(0.1、1.0和10μg/ml等)进行包被后,在其它试验条件相同时,观察阳性标本的OD值。选择OD值最大而蛋白量最少的浓度。对于多数蛋白质来说通常为1~10μg/ml。
(3) 酶标记抗体工作浓度的选择:首先用直接ELISA法进行初步效价的滴定(见酶标记抗体部份)。然后再固定其它条件或采取“方阵法”(包被物、待检样品的参考品及酶标记抗体分别为不同的稀释度)在正式实验系统里准确地滴定其工作浓度。
(4) 酶的底物及供氢体的选择:对供氢体的选择要求是价廉、安全、有明显地显色反应,而本身无色。有些供氢体(如OPD等)有潜在的致癌作用,应注意防护。有条件者应使用不致癌、灵敏度高的供氢体,如TMB和ABTS是目前较为满意的供氢体。底物作用一段时间后,应加入强酸或强碱以终止反应。通常底物作用时间,以10-30分钟为宜。底物使用液必须新鲜配制,尤其是H2O2在临用前加入。
1.固相载体的选择 载体的种类很多,其中包括纤维素、交联右旋糖酐、葡萄球菌聚苯乙烯、聚丙烯酰胺等。从使用形式上可有凹孔平板、试管、珠粒等。
聚苯乙烯凹孔板是应用最广泛的一种载体。聚苯乙烯塑料微量滴定板吸附蛋白的性能好,操作简便、用量小,适于大批检查。
由于聚苯乙烯的工艺过程不够稳定,造成各批次差异较大。所以进行ELISA之前,必须进行筛选。检查方法:
⑴ 吸附性能的检查:先加抗体包被,然后加入同一稀释度的酶标抗体,最后加底物、显色、测OD值,求出总平均OD值,再求出每相邻两孔的OD平均值,此均值在总均值的±10%以内为合格,若中间孔与四周孔OD值相差太大,或一侧与另一侧孔OD值相差较大均属不合格。
⑵ 对比测定阳性血清与阴性血清,观察是否存在明显差异,若二者OD值相差于10倍以上者为合格。
板的处理。新板一般不用处理,用蒸馏水冲洗即可应用。板用一次即废。但不少实验工作者认为用超声波处理,清洁液Tritonx100、20%乙二醇处理仍可应用。但发现空白对照显色较深和阳性样品显色结果不理想时,应弃去不用。
2.载体的吸附条件 载体的吸附均为物理吸附。吸附的多少取决于PH值、温度、蛋白浓度、离子强度以及吸附时间等。
较好的吸附条件是:离子强度为0.05Mol/L~0.10Mol/L,pH9.0~pH9.6碳酸盐缓冲液,蛋白浓度为1µg/ml~100µg/ml,4℃过夜或37℃3h。
3.酶标抗体使用浓度的确定 于聚苯乙烯板孔中加足够量的抗体包被,温育一定时间,冲洗、把酶标结合物倍比稀释,每个稀释度加2孔,温育、冲洗、再加底物显色、比色。以OD值为纵坐标,酶标结合物的稀释度为横坐标,制作曲线。找出OD值为1时,相对应的酶标抗体稀释度为最适酶标抗体稀释度。
这个稀释度是指在这种条件下的最适稀释度,换个条件就不是最适的了。如1﹕400的酶标抗体稀释度温育6h可与1︰6 400稀释度温育24h结果相同。所以一旦条件确定之后,就不要变更,以保证结果的重复性和相对的准确性。
此最适酶标抗体稀释度可做为工作浓度,也可提高半个至一个滴度,但不能提高过高,否则非特异性显色增加。
酶标抗体的滴度反映酶标抗体的质量,也可以此比较酶标结合物的优劣。有材料报道认为1︰320滴度为合格,1︰1 000以上更好。酶标抗体滴度越高,用于工作浓度的稀释倍数就越大,敏感性就越高,非特异性反应就越低。
4.抗原:
⑴ 抗原的要求:
用于ELISA的抗原必须采用相当纯的抗原,如果含有其它杂质,将与抗原共同竞争固相载体上的有限位置。用于其它血清学反应的抗原不一定能适用ELISA实验,必须经过试验,抗原必须能牢固地吸附于载体上,而不丧失其免疫活性,且可得到有规律的重复的结果。另外在吸附载体后,对加入的各种试剂产生最小的非特异性吸附,即与阴、阳性血清结合差异较大。
⑵ 抗原效价的测定 可采用单方阵或双方阵试验。①单方阵试验:以不同稀释度的抗原包被酶标板,以常规的1﹕200倍稀释的阳性血清加入,再加入酶标抗体、显色、测OD值,以OD值为1.0时,相应的抗原浓度作为使用效价;②双方阵试验比较精确,它既能测出抗原的最适浓度又能测出抗体的最适浓度。即将抗原抗体均稀释成不同浓度进行酶标抗体反应,以血清稀释倍数最高的阴、阳性血清的光吸收值差最大的所对应的抗原稀释度为抗原的使用效价。
已吸附的抗原的固相载体经冻干或干燥保存很稳定,数月仍不失活。
5.抗体 抗体效价的测定同抗原,采用双方阵试验。
6.清洗液 一般采用0.01Mol/L pH 7.2 PBS吐温缓冲液。吐温是聚氧乙烯去水山梨醇脂肪酸酯,为非离子型的表面张力物质,常做助溶剂。吐温的编号依聚合山梨醇所结合的脂肪酸种类不同而定。吐温20是结合月桂酸、吐温40是结合棕榈酸、吐温60是结合硬脂酸,吐温80是结合油酸等。通常用吐温20加入缓冲液内做为湿润剂,以减少非特异性吸附。也可在PBS缓冲液中加入1%牛血清白蛋白(或10%小牛血清或卵清蛋白),特别在抗原包被以后,以牛血清白蛋白缓冲液再包被一次,而占据孔内剩下位置,这样来减少非特异性反应。
7.反应时间 抗原与抗体、抗体与酶标抗体反应一般在37℃ 2h~3h达到高峰。时间太短,敏感性下降,时间太长,吸附的抗原或复合物(在这个温度下)可能脱落。
酶底物反应时间的确定:一般采用15min~30min~45min。也可以标准阳性血清为准,随时测定其OD值,当达到规定的OD值时,即终止反应。
(一)材料及试剂
1.猪瘟单抗纯化抗原
2.兔抗猪IgG酶标抗体
3.猪瘟阳性血清
4.猪瘟阴性血清
1~4均由指定的生物制品所购买。
5.ELISA反应板
6.包被液
碳酸钠 1.50g
碳酸氢钠 2.93g
H2O加至 1 000ml
pH值9.6
7.PBS液
氯化钠 8.90g
磷酸二氢钾 0.20g
无水磷酸氢二钠 2.13g
加双馏水 1 000ml
8.PBS-吐温洗涤液
PBS液 1 000ml
犊牛血清 5ml
混合即可
9.底物溶液
⑴ 0.1Mol/L柠檬酸液
柠檬酸 21g
双蒸馏水加至 1 000ml
⑵ 0.2Mol/L Na2HPO4液
Na2HPO4•12H2O 71.6g
双蒸馏水 加至 1 000ml
⑶ pH5.0磷酸盐-柠檬酸缓冲液
取⑴液 24.30ml
⑵液 25.70ml
混匀即可
⑷邻苯二胺液
取⑶液 50ml
双馏水 50ml
磷苯二胺 20mg
30%H2O2 0.15ml
待邻苯二胺溶化后再加H2O2,现用现配。
10.终止液
浓H2SO4(98%) 22.2ml
H2O 177.80ml
(二)操作方法
1.用包被液将猪瘟弱毒单抗纯化酶联抗原、猪瘟强毒单抗纯化酶联抗原各做100倍稀释,每孔包被100µl,4℃湿盒过夜。
2.次日取出,甩去孔内液体,3×3′冲洗。
3.将待检血清以PBS液做400倍稀释,每孔加100µl同时将猪瘟阳性血清、猪瘟阴性血清各做100倍稀释,于对照孔中加100μl。37℃温育1.5h~2h。
4.重复第二步,取出,甩去孔内液体,3×3′洗涤。
5.将兔抗猪IgG酶标抗体以PBS液做100倍稀释,每孔加100μl,37℃温育1.5h~2h。
6.重复第4步。
7.每孔加底物溶液100µl,室温下观察显色反应。当阴性对照孔稍显色时,立即终止反应,并以阴性孔做空白对照。
8.每孔加终止液50µl立即于酶联免疫吸附检测仪测定490nm波长的光密度。
(三)结果判定
在猪瘟弱毒酶联板上,OD≥0.2,为猪瘟弱毒抗体阳性;OD<0.2,为猪瘟弱毒抗体阴性。
在猪瘟强毒酶联板上,OD≥0.5,为猪瘟强毒抗体阳性;OD<0.2,为猪瘟强毒抗体阴性。
(一)材料与试剂
1.副结核分枝杆菌亲和层析抗原
2.草分枝杆菌吸收抗原
3.兔抗牛IgG酶标抗体
4.牛副结核病参考阳性血清
5.牛副结核病参考阴性血清
1~5项均由指定单位供应。
6.器材 ELISA板, 酶联免疫吸附检测仪、加样器、洗瓶、恒温箱等。
7.试剂及溶液配制同第五节猪瘟ELISA。
(二)操作方法
1.抗原包被 以抗原稀释液将副结核亲和层析抗原稀释至50µg/ml,每孔包被0.1ml。部分对照孔以牛血清白蛋白(50µg/ml)包被。
2.血清处理 取待检血清、参考阳性血清、参考阴性血清各0.10ml,加生理盐水0.80ml,加草分枝杆菌吸收抗原0.10ml,混匀,37℃感作1h。取0.10ml,加血清稀释液0.90ml(注意血清稀释液中加牛血清白蛋白,不加犊牛血清)。混匀即可
3.正式试验 按表12-4进行。每个样品加2孔,以求OD平均值。
表12-4 ELISA试验程序表(单位ml)
试验组 对照组
阳性对照 阴性对照 抗原对照 抗体对照 酶标抗体对照 底物对照
抗原包被 0.10 0.10 0.10 0.10
牛血清白蛋白包被 0.10 0.10 0.10
37℃感作3h,3×3min冲洗
待检血清 0.10
阳性血性 0.10 0.10
阴性血清 0.10
血清稀释液 0.10 0.10 0.10
37℃感作1.5h,3×3min冲洗
酶标抗体(工作浓度) 0.10 0.10 0.10 0.10 0.10 0.10
血清稀释液 0.10
37℃感作1.5h,3×3min冲洗
底物溶液 0.10 0.10 0.10 0.10 0.10 0.10 0.10
37℃或室温感作避光30min冲洗
2Mol/L H2SO4(滴) 1 1 1 1 1 1 1
(三)结果判定
在对照组成立的前提下, 即参考阳性血清呈棕黄色,参考阴性血清及其它对照孔呈无色或浅黄色, 判定待测结果。
1.目测判定 与参考阳性血清孔颜色相当,即呈棕黄色,判为ELISA阳性(+)。
2.酶标仪判定(490nm) 以底物溶液对照孔调零,校正参考阳性血清OD值为1.0(或相应规定值),测定待检孔。当OD≥0.50,判ELISA阳性(+);0.40≤OD≤0.49判ELISA可凝(±);OD<0.40,判ELISA阴性(-)。
优质的试剂,良好的仪器和正确的操作是保证ELISA检测结果准确可靠的必要条件。ELISA的操作因固相载体的形成不同而有所差异,国内医学检验一般均用板式点。本文将叙述板式ELISA各个操作步骤的注意要点,珠式、管式及磁性球ELSIA,国外试剂均与特殊仪器配合应用,两者均有详细的使用说明,严格遵照规定操作,必能得出准确的结果。
1 标本的采取和保存
可用作ELISA测定的标本十分广泛,体液(如血清)、分泌物(唾液)和排泄物(如尿液、粪便)等均可作标本以测定其中某种抗体或抗原成份。有些标本可直接进行测定(如血清、尿液),有些则需经预处理(如粪便和某些分泌物)。大部分ELISA检测均以血清为标本。血浆中除尚含有纤维蛋白原和抗凝剂外,其他成份均同等于血清。制备血浆标本需借助于抗凝剂,而血清标本只要待血清自然凝固、血块收缩后即可取得。除特殊情况外,在医学检验中均以血清作为检测标本。在ELISA中血浆和血清可同等应用。血清标本可按常规方法采集,应注意避免溶血,红细胞溶解时会释放出具有过氧化物酶活性的物质,以HRP为标记的ELISA测定中,溶血标本可能会增加非特异性显色。
血清标本宜在新鲜时检测。如有细菌污染,菌体中可能含有内源性HRP,也会产生假阳性反应。如在冰箱中保存过久,其中的可发生聚合,在间接法ELISA中可使本底加深。一般说来,在5天内测定的血清标本可放置于4℃,超过一周测定的需低温冰存。冻结血清融解后,蛋白质局部浓缩,分布不均,应充分混匀宜轻缓,避免气泡,可上下颠倒混和,不要在混匀器上强烈振荡。混浊或有沉淀的血清标本应先离心或过滤,澄清后再检测。反复冻融会使抗体效价跌落,所以测抗体的血清标本如需保存作多次检测,宜少量分装冰存。保存血清自采集时就应注意无菌操作,也可加入适当防腐剂。
2 试剂的准备
按试剂盒说明书的要求准备实验中需用的试剂。ELISA中用的蒸馏水或去离子水,包括用于洗涤的,应为新鲜的和高质量的。自配的缓冲液应用pH计测量较正。从冰箱中取出的试验用试剂应待温度与室温平衡后使用。试剂盒中本次试验不需用的部分应及时放回冰箱保存。
3 加样
在ELISA中一般有3次加样步聚,即加标本,加酶结合物,加底物。加样时应将所加物加在LEISA板孔的底部,避免加在孔壁上部,并注意不可溅出,不可产生气泡。加标本一般用微量加样器,按规定的量加入板孔中。每次加标本应更换吸嘴,以免发生交叉污染,也可用一次性的定量塑料管加样。有此测定(如间接法ELISA)需用稀释的血清,可在试管中按规定的稀释度稀释后再加样。也可在板孔中加入稀释液,再在其中加入血清标本,然后在微型震荡器上震荡1分钟以保证混和。加酶结合物应用液和底物应用液时可用定量多道加液器,使加液过程迅速完成。
4 保温
在ELISA中一般有两次抗原抗体反应,即加标本和加酶结合物后。抗原抗体反应的完成需要有一定的温度和时间,这一保温过程称为温育(incubation),有人称之为孵育,在ELISA中似不恰当。
ELISA属固相免疫测定,抗原、抗体的结合只在固相表面上发生。以抗体包被的夹心法为例,加入板孔中的标本,其中的抗原并不是都有均等的和固相抗结合的机会,只有最贴近孔壁的一层溶液中的抗原直接与抗体接触。这是一个逐步平衡的过程,因此需经扩散才能达到反应的终点。在其后加入的酶标记抗体与固相抗原的结合也同样如此。这就是为什么ELISA反应总是需要一定时间的温育。
温育常采用的温度有43℃、37℃、室温和4℃(冰箱温度)等。37℃是实验室中常用的保温温度,也是大多数抗原抗体结合的合适温度。在建立ELISA方法作反应动力学研究时,实验表明,两次抗原抗体反应一般在37℃经1-2小时,产物的生成可达顶峰。为加速反应,可提高反应的温度,有些试验在43℃进行,但不宜采用更高的温度。抗原抗体反应4℃更为彻底,在放射免疫测定中多使反应在冰箱中过夜,以形成最多的沉淀。但因所需时间太长,在ELISA中一般不予采用。
保温的方式除有的ELISA仪器附有特制的电热块外,一般均采用水浴,可将ELISA板置于水浴箱中,ELISA板底应贴着水面,使温度迅速平衡。为避免蒸发,板上应加盖,也可用塑料贴封纸或保鲜膜覆盖板孔,此时可让反应板漂浮在水面上。若用保温箱,ELISA板应放在湿盒内,湿盒要选用传热性良好的材料如金属等,在盒底垫湿的纱布,最后将ELISA板放在湿纱布上。湿盒应先放在保温箱中预温至规定的温度,特别是在气温较低的时候更应如此。无论是水浴还是湿盒温育,反应板均不宜叠放,以保证各板的温度都能迅速平衡。室温温育的反应,操作时的室温应严格限制在规定的范围内,标准室温温度是指20-25℃,但具体操作时可根据说明书的要求控制温育。室温温育时,ELISA板只要平置于操作台上即可。应注意温育的温度和时间应按规定力求准确。为保证这一点,一个人操作时,一次不宜多于两块板同时测定。
5 洗涤
洗涤在ELISA过程中虽不是一个反应步骤,但却也决定着实验的成败。ELSIA就是靠洗涤来达到分离游离的和结合的酶标记物的目的。通过洗涤以清除残留在板孔中没能与固相抗原或抗体结合的物质,以及在反应过程中非特异性地吸附于固相载体的干扰物质。聚苯乙烯等塑料对蛋白质的吸附是普遍性的,而在洗涤时又应把这种非特异性吸附的干扰物质洗涤下来。可以说在ELISA操作中,洗涤是最主要的关键技术,应引起操作者的高度重视,操作者应严格按要求洗涤,不得马虎。
洗涤的方式除某些ELISA仪器配有特殊的自动洗涤仪外,手工操作有浸泡式和流水冲洗式两种,过程如下:
(1)浸泡式 a.吸干或甩干孔内反应液;b.用洗涤液过洗一遍(将洗涤液注满板孔后,即甩去);c.浸泡,即将洗涤液注满板孔,放置1-2分钟,间歇摇动,浸泡时间不可随意缩短;d.吸干孔内液体。吸干应彻底,可用水泵或真空泵抽吸,也可甩去液体后在清洁毛巾或吸水纸上拍干;e.重复操作c和d,洗涤3-4次(或按说明规定)。在间接法中如本底较高,可增加洗涤次数或延长浸泡时间。
微量滴定板多采用浸泡式洗涤法。洗涤液多为含非离子型洗涤剂的中性缓冲液。聚苯乙烯载体与蛋白质的结合是疏水性的,非离子型洗涤剂既含疏水基团,也含亲水基团,其疏水基团与蛋白质的疏水基团借疏水键结合,从而削弱蛋白质与固相载体的结合,并借助于亲水基团和水分子的结合作用,使蛋白质回复到水溶液状态,从而脱离固相载体。洗涤液中的非离子型洗涤剂一般是吐温20,其浓度可在0.05%-0.2%之间,高于0.2%时,可使包被在固相上的抗原或抗体解吸附而减低试验的灵敏度。
(2)流水冲洗式 流水冲洗法最初用于小珠载体的洗涤,洗涤液仅为蒸馏水甚至可用自来水。洗涤时附接一特殊装置,使小珠在流水冲击下不断地滚动淋洗,持续冲洗2分钟后,吸干液体,再用蒸馏水浸泡2分钟,吸干即可。浸泡式犹如盆浴,流水冲洗式则好比淋浴,其洗涤效果更为彻底,且也简便、快速。已有实验表明,流水冲洗式同样也适用于微量滴定板的洗涤。洗涤时设法加大水流量或加大水压,让水流冲击板孔表面,洗涤效果更佳。
6 显色和比色
6.1 显色
显色是ELISA中的最后一步温育反应,此时酶催化无色的底物生成有色的产物。反应的温度和时间仍是影响显色的因素。在一定时间内,阴性孔可保持无色,而阳性孔则随时间的延长而呈色加强。适当提高温度有助于加速显色进行。在定量测定中,加入底物后的反应温度和时间应按规定力求准确。定性测定的显色可在室温进行,时间一般不需要严格控制,有时可根据阳性对照孔和阴性对照孔的显色情况适当缩短或延长反应时间,及时判断。
OPD底物显色一般在室外温或37℃反应20-30分钟后即不再加深,再延长反应时间,可使本底值增高。OPD底物液受光照会自行变色,显色反应应避光进行,显色反应结束时加入终止液终止反应。OPD产物用硫酸终止后,显色由橙黄色转向棕黄色。
TMB受光照的影响不大,可在室温中置于操作台上,边反应观察结果。但为保证实验结果的稳定性,宜在规定的适当时间阅读结果。TMB经HRP作用后,约40分钟显色达顶峰,随即逐渐减弱,至2小时后即可完全消退至无色。TMB的终止液有多种,叠氮钠和十二烷基硫酸钠(SDS)等酶抑制剂均可使反应终止。这类终止剂尚能使蓝色维持较长时间(12-24小时)不褪,是目视判断的良好终止剂。此外,各类酸性终止液则会使蓝色转变成黄色,此时可用特定的波长(450nm)测读吸光值。
6.2 比色
比色前应先用洁净的吸水纸拭干板底附着的液体,然后将板正确放入酶标比色仪的比色架中。以软板为载体的试验,需先将板置于标准96孔的座架中,才可进行比色。最好在加底物液显色前,先将软板边缘剪净,这样,此板就可完全平妥坐入座架中。 比色时应先以蒸馏水校零点,测读底物孔(未经任何反应仅加底物液的孔)和空白孔(以生理盐水或稀释液代替标本作全过程的孔),以记录本次试验的试剂状况。其后可用空白孔以蒸馏水校零点,以上各孔的吸光度需减去空白孔的吸光度,然后进行计算。
比色结果的表达以往通用光密度(oplical density,OD),现按规定用吸光度(absorbence,A),两者含义相同。通常的表示方法是,将吸收波长写于A字母的右下角,如OPD的吸收波长为492nm,表示方法为"A492nm"或"OD492nm"。
6.3 酶标仪
酶标比色仪简称酶标仪,通常指专用于测读ELISA结果吸光度的光度计。针对固相载体形式的不同,各有特制的适用于板、珠和小试管的设计。许多试剂公司配套供应酶标仪。酶标仪的主要性能指标有:测读速度、读数的准确性、重复性、精确度和可测范围、线性等等。优良的酶标仪的读数一般可精确到0.001,准确性为±1%,重复性达0.5%。举例说,若某孔测得的A值为1.083,则该孔相对于空气的真实A值应为1.083±0.01(1.073~1.093),重复测定数次,其A值均应1.083±0.05(1.078~1.088)在之间。酶标仪的可测范围视各酶标仪的性能而不同。普通的酶标仪在0.000~2.000,新型号的酶标
仪上限拓宽达2.900,甚至更高。超出可测上限的A值常以"*"或"over"或其它符号表示。应注意可测范围与线性范围的不同,线性范围常小于可测范围,比如某一酶标仪的可测范围为0.000~2.900,而其线性范围仅0.000~2.000,这在定量ELISA中制作标准曲线时应予注意。
酶标仪不应安置在阳光或强光照射下,操作时室温宜在15~30℃,使用前先预热仪器15-30分钟,测读结果更稳定。
测读A值时,要选用产物的敏感吸收峰,如OPD用492nm波长。有的酶标仪可用双波长式测读,即每孔先后测读两次,第一次在最适波长(W1),第二次在不敏感波长(W2),两次测定间不移动ELISA板的位置。例如OPD用492nm为W1,630nm为W2,最终测得的A值为两者之差(W1-W2)。双波长式测读可减少由容器上的划痕或指印等造成的光干扰。
各种酶标仪性能有所不同,使用中应详细新闻记者说明书。
7 结果判断
7.1 定性测定
定性测定的结果判断是对受检标本中是否含有待测抗原或抗体作出"有"或"无"的简单回答,分别用"阳性"、"阴性"表示。"阳性"表示该标本在该测定系统中有反应。"阴性"则为无反应。用定性判断法也可得到半定量结果,即用滴度来表示反应的强度,其实质仍是一个定性试验。在这种半定量测定中,将标本作一系列稀释后进行试验,呈阳性反应的最高稀释度即为滴度。根据滴度的高低,可以判断标本反应性的强弱,这比观察不稀释标本呈色的深浅判断为强阳性、弱阳性更具定量意义。
在间接法和夹心法ELSIA中,阳性孔呈色深于阴性孔。在竞争法ELISA中则相反,阴性孔呈色深于阳性孔。两类反应的结果判断方法不同,分述于下。
(1) 间接法和夹心法
这类反应的定性结果可以用肉眼判断。目视标本也无色或近于无色者判为阴性,显色清晰者为阳性。但在ELSIA中,正常人血清反应后常可出现呈色的本底,此本底的深浅因试剂的组成和实验的条件不同而异,因此实验中必须加测阴性对照。阴性对照的组成应为不含受检物的正常血清或类似物(见3.6)。在用肉眼判断结果时,更宜用显色深于阴性对照作为标本阳性的指标。
目视法简捷明了,但颇具主观性。在条件许可下,应该用比色计测定吸光值,这样可以得到客观的数据。先读出标本(sample,S)、阳性对照(P)、和阴性对照(N)的吸光值,然后进行计算。计算方法有多种,大致可分为阳性判定值法和标本与阴性对照比值法两类。
a. 阳性判定值
阳性判定值(cut-off value)一般为阴性对照A值加上一个特定的常数,以此作为判断结果阳性或阴性的标准。
用此法判断结果要求实验条件十分恒定,试剂的制备必须标准化,阳性和阴性的对照品应符合一定的规格,须配用精密的仪器,并严格按规定操作。阳性判定值公式中的常数是在这特定的系统中通过对大量标本的实验检测而得到的。现举某种检测HBsAg的试剂盒为例。试剂盒中的阴性对照品为不含HBsAg的复钙人血浆,阳性对照品HBsAg的含量标明为P=9±2ng/ml。每次试验设2个阳性对照和3个阴性对照。测得A值后,先计算阴性对照A值的平均数(NCX)和阳性对照A值的平均数(PCX),两个平均数的差(P-N)必须大于一个特定的数值(例0.400),试验才有效。3个阴性对照A值均应≥0.5×NCX,并≤1.5×NCX,如其中之一超出此范围,则弃去,而已另两个阴性对照重新计算NCX;如有两个阴性对照A值超出以上范围,则该次实验无效。阳性判定值按下式计算: 阳性判定值=NCX+0.05 标本A值>阳性判定值的为阳性,小于阳性判定值的为阴性。应注意的是,式中0.05为该试剂盒的常数,只适合于该特定条件下,而不是对各种试剂均可通用。
根据以上叙述可以看出,在这种方法中阴性对照和阳性对照也起到试验的质控作用,试剂变质和操作不当均会产生"试验无效"的后果。
b.标本/阴性对照比值
在实验条件(包括试剂)较难保证恒定的情况下,这种判断法较为合适。在得出标本(S)和阴性对照(N)的A值后,计算S/N值。也有写作P/N的,这里的P不代表阳性(positive),而是病人(patient)的缩写,不应误解。为避免混淆,更宜用S/N表示。在早期的间接法ELISA中,有些作者定出S/N为阳性标准,现多为各种测定所沿用。实际上每一测定系统应该用实验求出各自的S/N的阈值。更应注意的是,N所代表的阴性对照是不含受检物质的人血清。有的试剂盒中所设阴性对照为不含蛋白质或蛋白质含量较底的缓冲液,以致反应后产生的本底可能较正常人血清的本底低得多。因此,这类试剂盒规,如N<0.05(或其他数值),则按0.05计算,否则将出现假阳性结果。
(2)竞争法
在竞争法ELISA中,阴性孔呈色深于阳性孔。阴性呈色的强度取决于反应中酶结合物的浓度和加入竞争抑制物的量,一般调节阴性对照的吸光度在1.0-1.5之间,此时反应最为敏感。
竞争法ELISA不易用自视判断结果,因肉眼很难辨别弱阳性反应与阴性对照的显色差异,一般均用比色计测定,读出S、P和N的吸光值。计算方法主要也有两种,即阳性判定值法和抑制率法。
a. 阳性判定值法
与间接法和夹心法中的阳性判定值法基本相同,但在计算公式中引入阳性对照A值,现举某种检测抗HBc的试剂盒为例。试剂盒中的阴性对照为不含抗HBc的复钙人血浆,阳性对照中抗HBc含量为125±100u/ml。每次试验设2个阳性对照和3个阴性对照。测得A值后,先计算阴性对照A值的平均值(NCX)和阳性对照A值的平均数(PCX),两个平均数的差(N-P)必须大于一个特定的数值(例如0.300),试验才有效。3个阴性对照A值均应小于2.000,而且应≥0.5×NCX并≤1.5×NCX,如其中之一超出此范围,则弃去,而以另2个阴性对照重新计算×NCX;如有2个阴性对照A超出以上范围,则该次实验无效。阳性判定值按下式计算:
阴性判定值=0.4×NCX+0.6×PCX
标本A值≤阳性判定值的反应为阳性,A>阳性判定值的反应为阴性。
b. 抑制率法
抑制率表示标本在竞争结合中标本对阴性反应显色的抑制程度,按下式计算:
抑制率(%)= (阴性对照A值-标本A值)×100%/阴性对照A值
一般规定抑制率≥50%为阳性,<50%为阴性。
7.2 定量测定
ELSIA操作步骤复杂,影响反应因素较多,特别是固相载体的包被难达到各个体之间的一致,因此在定量测定中,每批测试均须用一系列不同浓度的参考标准品在相同的条件下制作标准曲线。测定大分子量物质的夹心法ELISA,标准曲线的范围一般较宽,曲线最高点的吸光度可接近2.0,绘制时常用半对数纸,以检测物的浓度为横坐标,以吸光度为纵坐标,将各浓度的值逐点连接,所得曲线一般呈S形,其头、尾部曲线趋于平坦,中央较呈直线的部分是最理想的检测区域。
测定小分子量物质常用竞争法,其标准曲线中吸光度与受检物质的浓度呈负相关。标准曲线的形状因试剂盒所用模式的差别而略有不同。
新型酶标仪一般带有自动软件可进行定量分析。
斑点-ELISA(dot-ELISA)的特点时:①以吸附蛋白质能力很强的硝酸纤维素膜为固相载体;②底物经酶反应后形成有色沉淀,使固相膜染色。在实验室中斑点-ELISA可按下法进行。在硝酸纤维膜上用铅笔划成4mm×4mm的小格,在每格中央点加抗原1~2μl,成为一个小点。干燥后将每格剪下分别放入ELISA板孔中,按ELISA方法操作,最后加入能形成不溶性有色沉淀的底物,如在膜上出现染色斑点,即为阳性反应。因硝酸纤维素膜吸附性能强,一般在包被后须再进行封闭。如将硝酸纤维素膜裁剪成膜条,并在同一张膜条上点有多种抗原,将整个膜条与同一份血清反应,则可同时获得对多种疾病的诊断结果。斑点-ELISA的缺点是操作麻烦,特别是洗涤的操作很不方便。
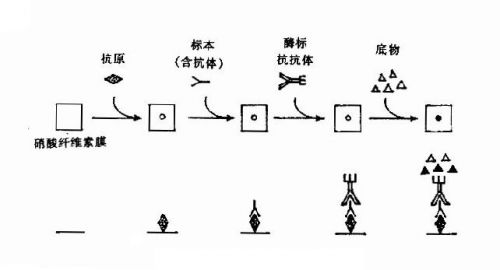 |
| 斑点-ELISA |
应用斑点-ELISA的原理,通过特殊工艺已制备出各种试剂,供临床检验用。一般分三种类型:①将试剂膜粘贴在塑料条片,便于洗涤和观察。②将试剂膜封在小盒内,膜下垫吸水剂,洗涤液通过膜吸入盒内。此即斑点免疫渗滤试验。③将试剂膜固定在小杠框格中放入特殊的自动分析仪中检测。应用这一系统可做各种蛋白质、激素、药物和抗生素的定量测定。
→如果您认为本词条还有待完善,请 编辑词条
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
2