
实验目的
了解IPTG诱导的外源基因在大肠杆菌中的表达的原理,掌握外源基因在大肠杆菌中的表达及其检测技术。
实验原理
将外源基因克隆在含有lac 启动子的表达载体中,让其在大肠杆菌中表达。没有加入IPTG诱导剂的时候,lacI 产生的阻遏蛋白与lac 操纵基因结合,从而不能进行外源基因的转录和表达,而只有表达载体随大肠杆菌的增殖和复制;当加入IPTG后,阻遏蛋白不能与操纵基因结合,则DNA外源基因大量转录并高效表达。表达的蛋白可以通过SDS-PAGE进行初步鉴定。
不同的蛋白质分子具有不同的电荷和分子量。蛋白质在强阴离子去污剂SDS与某一还原剂(如二巯基乙醇)共同作用下并加热使蛋白质解离后,变性的蛋白质与SDS结合并因此而带负电荷,不同的蛋白质结合SDS的量仅与分子量成正比而与氨基酸的序列无关,在SDS-PAGE电泳时,蛋白质在聚丙烯酰胺中的迁移率仅仅取决于蛋白质的分子量。
聚丙烯酰胺凝胶电泳由丙烯酰胺单体和交联剂N,N′—亚甲基双丙烯酰胺在催化剂作用下,形成三维网状结构。凝胶电泳不仅具有分辨不同分子量蛋白质的作用(即分子筛作用),还具有浓缩作用。由于不连续缓冲系统具有把样品中的SDS-多肽复合物全部浓缩于极小体积的能力,从而提高了分辨率。采用考马斯亮蓝快速染色,可及时观察电泳分离效果。
实验内容
材料:含有重组表达载体pET-B1, 空表达载体pET28b的大肠杆菌BL21。
试剂:细菌培养用的LB液体培养基,(含50μg/ml的卡那霉素)
LB平板(含50μg/ml的卡那霉素),100mMIPTG,
10mg/ml的溶菌酶(10mM Tris-HCl,pH8.0配制),
SDS-PAGE用试剂及考马斯亮蓝R250
30%(W/V)凝胶贮存液(丙烯酰胺具有神经毒性,操作时要戴手套和口罩)
丙烯酰胺29g,亚甲双丙烯酰胺1g, 加ddH2O溶至100ml,用新华3号滤纸过滤,棕色瓶中4℃保存,每隔几个月须重新配制。
Tris-HCl,pH8.8 1.5mol/L
0.5mol/L Tris—HCl,pH 6.8。
10%SDS。
10%过硫酸铵(AP,新鲜配制)。
TEMED(四甲基乙二胺)。
Tris-甘氨酸电泳缓冲液,pH8.3,可配成5×贮存液备用,临用前稀释。
工作液 5×贮存液
Tris碱 25 mmol/L Tris碱 15.1g
甘氨酸 250mmol/L (pH 8.3) 甘氨酸 94g
SDS 0.1% 1%SDS 50ml
加ddH2O 至1000ml
样品处理液
Deionized water 3.8 ml
0.5 M Tris-HCl, pH 6.8 1.0 ml
Glycerol 0.8 ml
10% (w/v) SDS 1.6 ml
2-mercaptoethanol 0.4 ml
1% (w/v) bromophenol blue 0.4 ml
染色液 0.4%考马斯亮蓝—R250染色液。
甲醇 400m1
冰乙酸 100ml
考马斯亮蓝R250 1g
ddH2O加至 1000m1
脱色液
甲醇 400ml
冰乙酸 100ml
ddH2O 500ml
操作步骤
1将冻存的含有组表达载体pET-B1, 空表达载体pET28b的大肠杆菌BL21画线接种在LB平板上,37度培养过夜,直至平板上长出单菌落。
2 挑取单菌落至5mlLB液体培养基中,培养至OD600=0.6左右。4度放置过夜。
3 取2ml培养菌加入到48ml培养基中,继续培养至OD600=0.4-0.6之间。
4 表达载体和重组载体都分别设置诱导组与不诱导组,诱导组加入终浓度为1mM的IPTG,不诱导组不加IPTG。25度诱导培养12h。
5 取1.5ml培养菌至离心管中,5000rpm离心1分钟,收集细菌。
6 用1ml 10mM Tris-HCl(pH8.0)悬浮细菌,5000rpm离心1分钟,收集细菌。
7 加入30ul的 10mg/ml的溶菌酶,充分悬浮,4度放置2小时以上。
8 制备4%浓缩胶,12%的分离胶的SDS-PAGE胶。
按下表制备浓缩胶
水 6.1
30%丙烯酰胺溶液 1.33
0.5mol/L Tris-HCl pH 6.8 2.5
10%SDS 0.1
10%AP 0.05
TEMED 0.01
按下表制备分离胶
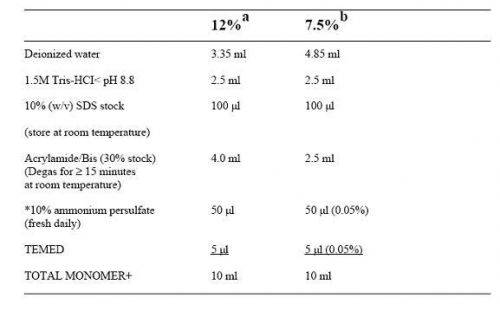 |
| 外源基因的表达与检测 |
结果: 诱导的pET-B1菌液样品在分子量61kDa处有一明显的深厚条带,而其他三种处理没有此条带。
影响蛋白质电泳分离效果的因素
1.蛋白质样品中的盐浓度 影响蛋白条带的迁移率和带型,因此为消除盐浓度的影响,溶解蛋白时最好用去离子水,再加等量2×SDS-PAGE样品缓冲液,必要时经过透析或进行Sephader G25过柱。
2.SDS的质量 由于变性蛋白是与SDS结合而带负电荷,蛋白结合SDS的量与蛋白质的分子量成正比,因此质量不同的SDS,相同的蛋白质样品,将可能出现不同迁移率的电泳图谱。
3.上样孔是否平齐,若上样孔不平齐,也影响蛋白电泳的迁移率。
4.为防止相邻泳道样品的扩散,而导致电泳条带的不整齐,如有空置的加样孔,须加等体积的空白1×SDS样品缓冲液。
电泳样品的准备
1.浓度 单一成分1—10μg,若浓度太稀,应沉淀后再进行电泳;对于非单一成分的样品,如基因工程大肠杆菌的表达产物,其蛋白量50~100μg可取得较好的分离效果。
2.体积 样品体积尽可能小,以保证电泳条带的整齐,必要时可应用6×SDS加样缓冲液以增加蛋白质的加样量。
3.盐浓度应尽可能低,可用SephaderG25快速脱盐;钾离子(K+)要除去,因为钾离子沉淀SDS。
4.分离小分子肽时,分离胶的浓度可提高到20%~25%。
5. 对照孔加入蛋白质分子量标准样品,同样也须1000C处理 3~5min。
注意事项
1. 丙烯酰胺单体和交联剂N,N′—亚甲基双丙烯酰胺有神经毒性,在称量和配制时要带一次性手套,称量时最好也戴上口罩。
2. 凝固后一般不再有毒性,但考虑到存在没有完全交连的分子,实验结束后不宜直接用手拿取,要先用清水漂洗5-10分钟。
3. 室温较低时胶液不易凝固,可以在槽中加370C温水。
4. SDS很容易漂浮在空气中而吸入体内,称量时最好在通风橱中进行,或戴上口罩。
5. 在实际操作中,很容易将电极接反,请注意,负极永远接在加样孔的一端(即上负下正)。
实验目的
掌握真核细胞的培养,细胞转染以及western blot 技术检测外源基因在哺乳细胞中的表达。
实验原理
哺乳动物细胞作为宿主表达系统具有许多优点:
(1) 该体系能识别和除去外源基因的内含子,剪接加工成熟的mRNA。
(2) 能对翻译后的蛋白质进行加工修饰,使表达产物具有生物活性。
(3) 用作受体的哺乳动物细胞易被重组DNA转染,其有遗传稳定性和可重复性。
哺乳动物基因转移载体都附有标记基因,以便于转染外源基因的细胞的筛选。外源DNA导入真核细胞的方法,常用的由磷酸钙转染法,电穿孔转染,脂质体包裹转染,显微注射及DEAE-葡聚糖转染技术。基因表达产物的检测可采用免疫荧光抗体,免疫沉淀及免疫印迹等方法进行。
实验内容
材料
质粒: pNTE-EGFP( 增强型绿色荧光蛋白标签的NTE全长表达载体)pEGFP-N3(Clontech);
哺乳动物细胞COS7
试剂
细胞培养试剂:DMEM (Gibco);胎牛血清(Hyclone)
抗生素:氨苄青霉素钠盐,硫酸链霉素(Sigma); G418(Gibco)
细胞转染试剂:Lipofectamine 2000 (Invitrogen);Opti-MEM I培养基(Gibco)
DNA纯化试剂盒:Endofree Plasmid Maxi Kit,Plasmid Midi Kit(Qiagen)
Western 试剂:抗体:BD Living Colors A. v. monoclonal antibody (JL-8) (BD Biosciences, Clontech);Anti-mouse IgG (Fc specific) peroxidase conjugate,Monoclonal anti-HA clone HA-7 (Sigma);人杂交膜Hybond ECL(Amersham);ECL底物:Supersignal West Pico Chemiluminescent Substrate (Pierce); X光片(柯达公司)
操作步骤
细胞的培养
COS7细胞在含有10%胎牛血清的DMEM,5%CO2,饱和湿度下培养。
转染用DNA的纯化
按照Qiagen 试剂盒说明书进行,测定DNA的浓度和纯度。
细胞的转染
转染前一天,接种细胞到无任何抗生素的DMEM培养基的6孔细胞培养板中,使细胞密度保持在90%饱和度。
将4 g DNA和10 l转染试剂Lipofectamine 2000分别溶于250 l无抗生素和血清的opti-MEMI培养基中,温和混匀,室温放置5分钟。
将稀释的DNA和转染试剂温和混匀,室温孵育20分钟。
将DNA和转染试剂的混合物加入到2 ml无抗生素的DMEM培养基中,前后来回摇晃混匀后,37℃培养48小时,直接进行蛋白的表达检测。
检测方法一:显微观察
由于表达的基因是与绿色荧光蛋白想欧联的,因此可以在转染48h后直接在荧光显微镜下观察,如果细胞发出绿色荧光,说明外源基因在其中表达。
检测方法二:Western blotting
细胞蛋白的提取和定量
转染后的培养细胞在吸去培养基之后,用胰酶消化经离心后收集细胞。用PBS漂洗2遍后,离心收集细胞,加入一定量的细胞总蛋白裂解液(20 mM MOPS,0.15 M NaCl,1% NP-40,1% 去氧胆酸钠,1 mM EDTA,1% SDS)。在加入裂解液和蛋白酶抑制剂(1 mM PMSF、10 g/ml Aprotinin、2 g/ml Leupetin、2 g/ml Benzamodine)之后,充分悬浮细胞,冰上超声破碎细胞,12000g 离心10分钟,取上清作为细胞蛋白提取物,用Lowry法测定蛋白浓度。
蛋白质的SDS-PAGE
等量的蛋白(40 g)在加入上样缓冲液充分混匀后,沸水浴煮5分钟,瞬时离心后进行SDS-PAGE。
蛋白印迹
将电泳后的蛋白胶在转移液(3.03 g Tris,14.4 g Glycine,200ml Methanol/L)中浸泡至少20分钟;Hybond ECL 膜在双蒸水中浸湿后,在转移液中平衡至少10分钟。半干转移法(BIO-RAD)转移3小时。
封阻和杂交
将印迹后的蛋白膜在封阻液(含5% 脱脂奶粉和 0.1%(V/V)Tween-20的PBS ,pH 7.5)中室温下封阻至少一小时。用洗液(含0.1%(V/V)Tween-20的PBS)稍洗两次后,再洗15分钟,1次;5分钟,2次。加入适量稀释的一抗,在4℃孵育杂交过夜。杂交后按照上述洗涤步骤洗膜。加入按1:1000稀释的二抗(偶联有辣根过氧化物酶的抗小鼠IgG抗体),在室温下孵育杂交至少1小时。按上述洗涤步骤洗膜。
化学发光曝光和显影
按10平方厘米1毫升检测液,等比例混合ECL检测液A和B,滴加在膜的蛋白面,室温放置5分钟,吸掉过多的检测液,用保鲜膜包裹膜(注意排除气泡),蛋白面朝上,黑暗下进行X光片曝光,按显影—停影—定影步骤冲洗胶片。
蛋白浓度测定(Lowry检测法)
先配制溶液A(100ml 含0.5g CuSO4•5H2O,1g 柠檬酸)和溶液B( 1L 含20g 碳酸钠,4g 氢氧化钠)。用双蒸水稀释样品至0.5 ml,然后加入2.5 ml 溶液C(1体积溶液A和50体积溶液B的混合物)混匀,在室温下放置5分钟-10分钟。接着加入0.25 ml 溶液D(等体积的Folin-酚和双蒸水的混合物),混匀。最后室温放置20分钟-30分钟后,在分光光度计上测A750 值。
蛋白质浓度标准曲线的制作:以牛血清白蛋白(BSA)为标准蛋白,0、2.5、5、10、20、40、80 g/ml的浓度蛋白制作,每个浓度设定3个重复,取平均光吸收值作为纵轴,蛋白浓度为横轴,绘制标准曲线。
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
0