
内分泌系统是由内分泌腺和分解存在于某些组织器官中的内分泌细胞组成的一个体内信息传递系统,它与神经系统密切联系,相互配合,共同调节机体的各种功能活动,维持内环境相对稳定。
人体内主要的内分泌腺有垂体、甲状腺、甲状旁腺、肾上腺、胰岛、性腺、松果体和胸腺;散在于组织器官中的内分泌细胞比较广泛,如消化首粘膜、心、肾、肺、皮肤、胎盘等部位均存在于各种各样的内分泌细胞;此外,在中枢神经系统内,特别是下丘存在兼有内分泌功能的神经细胞。由内分泌腺或散在内分泌细胞所分泌的高效能的生物活性物质,经组织液或血液传递而发挥其调节作用,此种化学物质称为激素(hormone)。
随着内分泌研究的发展,关于激素传递方式的认识逐步深入。大多数激素经血液运输至远距离的靶细胞而发挥作用,这种方式称为远距分泌(telecring);某些激素可不经血液运输,仅由组织液扩散而作用于邻近细胞,这种方式称为旁分泌(paracrine);如果内分泌细胞所分泌的激素在局部扩散而又返回作用于该内分泌细胞而发挥反馈作用,这种方式称为自分泌(autocrine)。另外,下丘脑有许多具有内分泌功能的神经细胞,这类细胞既能产生和传导神经冲动,又能合成和释放激素,故称神经内分泌细胞,它们产生的激素称为神经激素(neurohormone)。神经激素可沿神经细胞轴突借轴浆流动运送至末梢而释放,这种方式称为神经分泌(neurocrine)。
一、激素的分类
激素的种类繁多,来源复杂,按其化学性质可分为两大类:
(一)含氮激素
1.肽类和蛋白质激素 主要有下丘脑调节肽、神经垂体激素、腺垂体激素、胰岛素、甲状旁腺激素、降钙素以及胃肠激素等。
2.胺类激素 包括肾上腺素、去甲肾上腺素和甲状腺激素。
(二)类固醇(甾体)激素
类固醇激素是由肾上腺皮质和性腺分泌的激素,如皮质醇、醛固酮、雌激素、孕激素以及雄激素等。另外,胆固醇的衍生物棗1,25-二羟维生素D3也被作为激素看待。
此外,前列腺素广泛存在于许多组织之中,由花生四烯酸转化而成,主要在组织局部释放,可对局部功能活动进行调节,因此可将前列腺看作一组局部激素。
主要激素及其化学性质
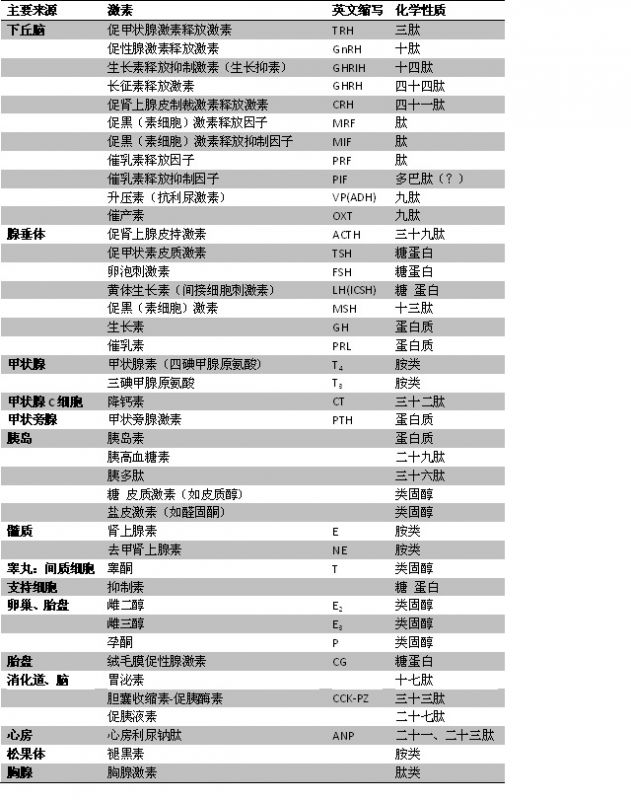 |
| 内分泌系统 |
二、激素作用的一般特性
激素虽然种类很多,作用复杂,但它们在对靶组织发挥调节作用的过程中,具有某些共同的特点。
(一)激素的信息传递使用
内分泌系统与神经系统一样,是机体的生物信息传递系统,但两者的信息传递形式有所不同。神经信息在神经纤维上传输时,以电信号为信息的携带者,在突触或神经-效应器接头外处,电信号要转变为化学信号,而内分泌系统的信息只是把化学的形式,即依靠激素在细胞与细胞之间进入信息传递。不论是哪种激素,它只能对靶细胞的生理化过程起加强或减弱的作用,调节其功能活动。例如,生长素促进生长发育,甲状腺激素增强代谢过程,胰岛素降低血糖等。在这些作用中,激素既不能添加成分,也不能提供能量,仅仅起着“信使”的作用,将生物信息传递给靶组织,发挥增强或减弱靶细胞内原有的生理化生化近程的作用。
(二)激素作用的相对特异性
激素释放进入血液被运送到全身各个部位,虽然他们与各处的组织、细胞有广泛接触,但有此激素只作用于某些器官、组织和细胞,这称为激素作用的特异性。被激素选择作用的器官、组织和细胞,分别称为靶器官、靶组织和靶细胞。有些激素专一地选择作用于某一内分泌腺体,称为激素的靶腺。激素作用的特异性与靶细胞上存在能与该激素发生特异性结合的受体有关。肽类和蛋白质激素的受体存在于靶细胞膜上,而类固醇激素与甲状腺激素的受体则位于细胞浆或细胞核内。激素与受体相互识别并发生特异性结合,经过细胞内复杂的反应,从而激发出一定的生理效应。有些激素作用的特异性很强,只作用于某一靶腺,如促甲状腺激素只作用于甲状腺,促肾上腺皮质激素只作用于肾上腺皮质,而垂体促性腺激素只作用于性腺等。有些激素没有特定的靶腺,其作用比较广泛,如生长素、甲状腺激素等,它们几乎对全身的组织细胞的代谢过程都发挥调节作用,但是,这些激素也是与细胞的相应受体结合而起作用的。
(三)激素的高效能生物放大作用
激素在血液中的浓度都很低,一般在纳摩尔(n mol/L),甚至在皮摩尔(p mol/L)数量级,虽然激素的含量甚微,但其作用显著,如1mg的甲状腺激素可使机体增加产热量约4200000 J(焦耳)。激素与受体结合后,在细胞内发生一系列酶促放大作用,一个接一个,逐级放大效果,形成一个效能极市制生物放电系统。据估计,一个分子的胰高血糖素使一个分子的腺苷酸环化酶激活后,通过cAMP-蛋白激酶。可激海参10000个分子的磷酸化酶。另外,一个分子的促甲状腺激素释放激素,可使腺垂体释放十万个分子的促甲状腺激素。0.1μg的促肾上腺皮质激素释放激素,可引起腺垂体释放1μg促肾上腺皮持激素,后者能引起肾上腺皮质分泌40μg糖 皮质激素,放大了400倍。据此不难理解血中的激素浓度虽低,但其作用却非常明显,所以体液中激素浓度维持相对的稳定,对发挥激素的正常调节作用极为重要。
(四)激素间的相互作用
当多种激素共同参与某一生理活动的调节时,激素与激素之间往往存在着协同作用或拮抗作用,这对维持其功能活动的相对稳定起着重要作用。例如,生长素、肾上腺素、糖皮质激素及胰高血糖素,虽然使用的环节不同,但均能提高血糖,在升糖效应上有协同作用;相反;胰岛素则以降低血糖,与上述激素的升糖效应有拮抗作用。甲状旁腺激素与1,12-二羟维生素D3对血钙的调节是相辅相成的,而降钙素则有拮抗作用。激素之间的协同作用与拮抗作用的机制比较复杂,可以发生在受体水平,也可以发生在受体后信息传递过程,或者是细胞内酶促反应的某一环节。例如,甲状腺激素可使许多组织(如心、脑等)β-肾上腺素能受体增加,提高对儿茶酚胺的敏感性,增强其效应。孕酮与醛固醛在受体水平存在着拮抗作用,虽然孕酮与醛固酮受体的亲和性较小,但当孕酮浓度升高时,则可与醛固酮竞争同一受体,从而减弱醛固酮调节水盐代谢的作用。前列环素(PGI2)可使血小板内cAMP增多,从而抑制血小板聚集;相反,血栓素A2(TXA2)却能使血小板内cAMP减少,促进血小板的聚集。
另外,有的激素本身并不能直接对某些器官、组织或细胞产生生理效应,然而在它存在的条件下,可使另一种激素的作用明显增强,即对另一种激素有调节起支持作用。这种现象称为允许作用(permissive action)。糖皮质激素的允许作用是最明显的,它对心肌和血管平滑肌并元收缩作用,但是,必须有糖皮质激素有存在,儿茶酚胺才能很好地发挥对心血管的调节作用。关于允许作用的机制,至今尚未完全清楚。过去认为,允许作用是由于糖皮质激素抑制儿茶酚-O-甲基移位酶,使儿茶酚胺降解速率减慢,导致儿茶酚胺作用增强。现在通过对受体和受体水平的研究,也可以调节受体介导的细胞内住处传递过程,如影响腺苷酸环化酶的活性以及cAMP的生成等。
三、激素作用的机制激素作为信息物质与靶细胞上的受体结合后,如何把信息传递到细胞内,并经过怎样的错综复杂的反应过程,最终产生细胞生物效应的机制,一直是内分泌学基础理论研究的重要领域。近一二十年来,随着分子生物学的发展,关于激素作用机制的研究,获得了迅速进展,不断丰富与完善了关于激素作用机制的理论学说。激素按其化学性质分为两在类棗含氮激素和类固醇激素,这两类激素有作用机制也完全不同。
(一)含氮激素有作用机制棗第二信使学说
第二信使学说是Sutherland等于1965年提出来的。Sutherland学派在研究糖原酵解第一步所需限速酶棗磷酸化酶的活性时,发胰高血糖素与肾上腺素可使肝匀浆在APT、Mg2+与腺苷酸环化酶(adenylate cyclase,AC)的作用下产生一种新物质,这种物质具有激活磷酸体酶从而催化糖原酵解的作用。实验证明,它是环-磷腺苷(cyclic AMP,cAMP),在Mg2+存在的条件下,腺苷酸化酶促进ATPA转变为cAMP。CAMP在磷酸二酯酶(phosphodiesterase)的作用下,降解为5ˊAMP。随后,进一步发现cAMP之所以能激活磷酸化酶,是由于cAMP激活了另一种酶,即依赖cAMP的蛋白激酶(cAMP-dependent protein kinase,cAMP-PK,PKA)而完成的。
Sutherland综合这些资料提出第二信使学说,其主要内容包括:①激素是第一信使,它可与靶细胞膜上具有立体构型的专一性受体结合;②激素与受体结合后,激活漠上的腺苷酸环化酶系统;③在mg2+楔存在的条件下,腺苷酸环化酶促使ATP转变为cAMP,cAMP是第二信使,信息由第一信使传递给第二信使;④cAMP是使无活性的蛋白激酶(PKA)激活。PKA具有两个亚单位,即调节亚单位与催化亚单位。CAMP与PKA的调节亚单位结合,导致调节亚单位与催化亚脱离而使PKA激活,催化细胞内多种蛋白质发生磷酸化反应,包括一些蛋白发生磷酸化,从而引起靶细胞各种生理生化反应。
以cAMP为第二信使学说的指出,推动了激素作用机制的研究工作迅速深入发展。近年来的研究资料表明,cAMP并不是唯一的第二信使,可能作为第二信使的化学物质还有cGMP、三磷酸肌醇、二酰甘油、Ca2+ 等。另外,关于细胞表现受体调节、腺苷酸环化酶活化机制、蛋白激酶C的作用等方面的研究都取得了很大进展,现概述如下:
1.激素与受体的相互作用 激素有膜受体多为糖蛋白,其结构一般分为三部分:细胞膜外区段、质膜部分和细胞膜内区段。细胞膜外区段含有许多糖基,是识别激素并与之结合的部位。激素分子和靶细胞受体的表现,均由许多不对称的功能基团构成极为复杂而又可变的立体构型。激素和受体可以相互诱导而改变本身的构型以适应对方的构型,这就为激素与受体发生专一性结合提供了物质基础。
激素与受体的结合力称为亲和力(affinity)。一般来说,由于相互结合是激素作用的第一步,所以亲和力与激素的生物学作用往往一致,但激素的类似物可与受体结合而不表现激素的作用,相反却阻断激素与受体相结合。实验证明,亲和力可以随生理条件的变化而发生改变,如动物性周期的不同阶段,卵巢颗粒细胞上的的卵泡刺激素(FSH)受体的亲和力是不相同的。某一激素与受体结合时,其邻近受体的亲和力也可出现增高或降低的现象。
受体除表现亲和力改变外,其数量也可发生变化。有人用淋巴细胞膜上胰岛素受体进行观察发现,如长期使用大剂量的胰岛素,将出现胰岛素受体数量减少,亲和力也降低;当把胰岛素的量降低后,受体的数量和亲和力可恢复正常。许多种激素(如促甲状腺激素、绒毛膜促性腺激素、黄体生成素、卵泡刺激素等)都会出现上述情况。这种激素使其特异性受体数量减少的现象,称为减衰调节或简称下调(down regulation0)。下调发生的机制可能与激素-受体复合物内移入胞有关。相反,有些激素(多在剂量较小时)也可使其特异性受体数量增多,称为上增调节或简称上调(up regulation),如催乳素、卵泡刺激素、血管紧张素等都可以出现上调现象。下调或上调现象说明,受体或上调现象说明,受体的合成与降解处于动态平衡之中,其数量是这一平衡的结果,它的多少与激素有量相适应,以调节靶细胞对激素有敏感性与反应强度。
2.G蛋白在信息传递中的作用 激素受体与腺苷酸环化酶是细胞膜上两类分开的蛋白质。激素受体结合的部分在细胞膜的外表面,而腺苷环化酶在膜的胞浆面,在两者之间存在一种起耦联作用的调节蛋白——鸟苷酸结合蛋白(guanine nucleotide-binding regulatory protein),简称G蛋白。G蛋白由α、β和γ三个亚单位组成,α亚单位上有鸟苷酸结合位点。当G蛋白上结合的鸟苷酸为GTP时则激活而发挥作用,但当G蛋白上的GTP水解为GDPA时则失去活性。当激素与受体结合时,活化的受体便与G蛋白的α亚单位结合,并促使其与β、γ亚单位脱离,才能对腺苷酸环化酶起激活或抑制作用。
G蛋白可分为兴奋型G蛋白(Gs)和抑制型G蛋白 Gi。Gs的作用是激活腺苷酸环化酶,从而使cAMP生成增多;Gi的作用则是抑制腺苷酸环化酶的活性,使cAMP生成减少。有人提出,细胞膜的激素受体也可分为兴奋型(Rs)与抑制型(Ri)两种,它们分别与兴奋性激素(Hs)或抑制性激素(Hi)发生结合,随后分别启动Gs或 Gi,再通过激活或抑制腺苷酸环化酶使cAMP增加或减少而发挥作用。
3.三磷酸肌醇和二酰甘油为第二信使的信息传递系统 许多含氮激素是以cAMP为第二信使调节细胞功能活动的,但有些含氮激素的作用信息并不以cAMP为媒介进行传递,如胰岛素、催产素、催乳素、某些下丘脑调节肽和生长因子等。实验证明,这些激素作用于膜受体后,往往引起细胞膜磷脂酰肌醇转变成为三磷酸肌醇(inositol-1,4,5,triphosphate,IP3)和二酰甘油(diacylglycerol,DG),并导致胞浆中Ca2+浓度增高。近年来,有人提出IP3和DG可能是第二信使的学说引起人们的重视,并且得到越来越我的实验证实。这一学说认为,在激素的作用下,可能通过G蛋白的介导,激活细胞膜内的磷脂酶C(phosphinositol-specific phospholipase C.PLC),它使由磷脂酰肌醇(PI)二次磷酸化生成的磷脂酰二磷肌醇(PIP2)分解,生成 IP3和DG。DG生成后仍留在膜中,IP3则进入胞浆。在未受到激素作用时,细胞膜几乎不存在游离的DG,细胞内IP3的含量也极微,只有在细胞3受到相应激素作用时,才加速PIP2的降解,大量产生 IP3和DG。IP3的作用是促使细胞内Ca2+贮存库释放Ca2+进入 胞浆。细胞内Ca2+主要贮存在线粒体与内质网中。实验证明,IP3引起Ca2+的释放是来自内质网而不是线粒体,因为在内质网膜上有IP3受体,IP3与其特异性受体结合后,激活Ca2+通道,使Ca2+从内质网中进入胞浆。IP3诱发Ca2+动员 最初发反应是引起暂短的内质网释放Ca2+,随后是由Ca2+释放诱发作用较长的细胞外Ca2+内流,导致胞浆中Ca2+浓度增加。Ca2+与细胞内的钙调蛋白(calmodulin,CaM)结合后,可激活蛋白酶,促进蛋白质磷酸化,从而调节细胞的功能活动。
DG的作用主要是它能特异性激活蛋白激酶C(protein kinase C,PKC)PKC的激活依赖于Ca2+的存在。激活的PKC与PKA一样可使多种蛋白质或酶发生磷酸化反应,进而调节细胞的生物效应。另外,DG的降解产物花生四烯酸是合成前列腺素的原料,花生四烯酸与前列腺素的过氧化物又参与鸟苷酸环化酶的激活,促进cGMP的生成。CGMP作为另一种可能的第二信使,通过激活蛋白激酶G(PKG)而改变细胞的功能。
(二)类固醇激素作用机制棗基因表达学说
因固醇激素的分子小(分子量仅为300左右)、呈脂溶性,因此可透过细胞膜进入细胞。在进入细胞之后,经过两个步骤影响基因表面而发挥作用,故把此种作用机制称为二步作用原理,或称为基因表达学说。
第一步是激素与胞浆受体结合,形成激素-胞浆受体复合物。在靶细胞将中存在着类固醇激素受体,它们是蛋白质,与相应激素结合特点是专一性强、亲和性大。例如,子宫组织胞浆的雌二醇受体能与17β-雌二醇结合,而不能与17α-雌二醇结合。激素与受体的亲和性大小与激素的作用强度是平行的。而且胞浆受体的含量也随靶器官的功能状态的变化而发生改变。当激素进入细胞内与胞浆受体结合后,受体蛋白发生构型变化,从而命名激素-胞浆受体复合物获得进入核内的能力,由胞浆转移至核内。第二步是与核内受体相互结合,形成激素-核受体复合物,从而激发DNA的转录过程,生成新的mRNA,诱导蛋白质合成,引起相应的生物效应。
近年来由于基因工程技术的发展与应用,不少类固醇激素的核内受体的结构已经清楚。它们是特异地对转录起调节作用的蛋白,其活性受因固醇激素的控制。核受体主要有三个功能结构域:激素结合结构域、DNAA结构结构域和转录增强结构域。一旦激素与受体结合,受体的分子构象发生改变,暴露出隐蔽于分子内部的DNA结合结构域及转录增强结构域,使受体DNA结合,从而产生增强转录的效应。另外,政治家实验资料表明,在DNA结合结构域可能有一个特异序列的氨基酸片断,它起着介导激素受体复合物与染色质中特定的部位相结合,发挥核定位信号的作用。
甲状腺激素虽属含氮激素,但其作用机制却与类固醇激素相似,它可进入细胞内,但不经过与胞浆受体结合即进入核内,与核受体结合调节基因表达。
应该指出,含氮激素可作用于转录与翻译阶段而影响蛋白质的合成;反过来,类固醇激素也可以作用于细胞膜引起基因表达学说难以解释的某引起现象。
下丘脑与神经垂体和腺垂体的联系非常密切,如视上核和室旁核的神经元轴突延伸终止于神经垂体,形成下丘脑-垂体束。在下丘脑与腺垂体之间通过垂体门脉系统发生功能联系。下丘脑的一些神经元既能分泌激素(神经激素),具有内分泌细胞的作用,又保持典型神经细胞的功能。它们可将从大脑或中枢神经系统其他部位传来的神经信息,转变为激素的信息,起着换能神经元的作用,从而以下丘脑为枢纽,把神经调节与体液调节紧密联系起来。所以,下丘脑与垂体一起组成下丘脑-垂体功能单位。
凡是能分泌神通肽或肽类激素的神经分泌细胞称为肽能神经元。下丘脑的肽能神经元主要丰硕盱视上核、室旁核与促垂体核团。促垂体区核团位于下丘脑的内侧基底部,主要包括正中隆起、弓状核、腹内侧核、视交叉上核以及室周核等,多属于小细胞肽能神经元,其轴突投射到正中隆起,轴突末梢与垂体门脉系统的第一级毛细血管风接触,可将下丘脑调节肽释放进入门脉系统,从而调节垂体的分泌活动。
一、下丘脑调节肽
下丘脑促垂体区肽能神经元分泌的肽类激素,主要作用是调节腺垂体的活动,因此称为下丘脑调节肽(hypothalamus regulatory peptide,HRP)。近20多年来,从下丘脑组织提取肽类激素获得成功,并已能人工合成。1968年Guillemin实验室从30万只羊的下丘脑中成功地分离出几毫克的促甲状腺激素释放激素(TRH),并在一年后确定其化学结构为三肽。在这一生成成果 鼓舞下,Schally实验室致力于促性腺激素释放激素(GnRH)的提取工作。1971年他们从16万头猪的下丘脑中提纯出GnRH,又经过6年的研究,阐明其化学结构为十肽。此后,生长素释放抑制激素 (GHRIH)、促肾上腺皮质激素释放激素(CRH)与生长素释放激素(GHRH)相继分离成功,并确定了化学结构,此外,还有四种对腺垂体催乳素和促黑激素的分泌起促进或抑制作用的激素,因尚未弄清其化学结构,所以暂称因子。
下丘脑调节肽除调节腺垂体功能外,它们几乎都具有垂体外作用,而且它们也不仅仅在下丘脑“促垂体区”产生,还可以大中枢神经系统其他部位及许多组织中找到它们踪迹,使人们更加广泛深入地研究他们的作用。
(一)促甲状腺激素释放激素
促甲状腺激素释放激素(thyrotropin-releasing hormone,TRH)是三肽,其化学结构为:
(焦)谷-组-脯-NH2
TRH主要作用于腺垂体促进促甲状腺激素(TSH)释放,血中T4和T3随TSH浓度上升而增加。给人和动物静脉注射TRH(1mg),1-2min内血浆TSH浓度便开始增加,10-20min达高峰,TSH的含量可增加20倍。腺垂体的促甲状腺激素细胞的膜上的TRH受体,与TRH结合后,通过Ca2+介导引起TSH释放,因此IP3-DG系统可能是TRH发挥作用的重要途径。TRH除了刺激腺垂体释放TSH外,也促进催乳互的释放,但TRH是否参与催乳素分泌的生理调节,尚不能肯定。
下丘脑存在大量的TRH神经元,它们主要分布于下丘脑中间基底部,如损毁下丘脑的这个区域则引起TRH分泌减少。TRH神经元合成的TRH通过轴浆运输至轴突末梢贮存,延伸到正中隆起初级毛细血管周围的轴突末梢在适当刺激作用下,释放TRH并进入垂体门脉系统运送到腺垂体,促进TRH释放。另外,在第三脑室周围尤其是底部排列有形如杯状的脑室膜细胞(tanycyte),其形态特点与典型的脑室膜细胞有所不同,其胞体细长,一端面向脑室腔,其边界上无纤毛而有突起,另一端则延伸至正中隆起的毛细血管周围。在这些细胞内含有大量的TRH与GnRH等肽类激素。下丘脑特别是室周核释放的TRH或GnRH进入第三脑室的脑脊液中,可被脑室膜细胞摄入,再转幸福至正中隆起附近释放,然后进入垂体门脉系统。
除了下丘脑有较多的TRH外,在下丘脑以外的中枢神经部位,如大脑和脊髓,也发现有TRH存在,其作用可能与神经信息传递有关。
(二)促性腺激素释放激素
促性腺激素释放激素(gonadotropin-releasing hormone,GnRH,LRH)是十肽激素,其化学结构为:
(焦)谷-组-色-丝-酪-甘-亮-精-脯-甘-NH2
GnRH促进性腺垂体合成与释放促性腺激素。当机体静脉注射100mgGnRH,10min后血中黄体生成素(LH)与卵泡刺激素(FSH)浓度明显增加,但以LH的增加更为显著。在体外腺垂体组织培养系统中加入GnRH,亦能引起LH与FSH分泌增加,如果先用GnRH抗血清处理后,再给予GnRH,则可减弱或消除GnRH的效应。
下丘脑释放GnRH的特脉冲式释放,因而造成血中LH与FSH浓度也呈现脉冲式波动。从恒河猴垂体门脉血管收集的血样测定GnRH含量,呈现阵发性时高时低的现象,每隔1-2h波动一次。在大鼠,GnRH每隔20-30min释放一次,如果给大鼠注射抗GnRH血清,则血中LH与FSH浓度的脉冲式波动消失,说明血中LH与FSH的脉冲式波动是由下丘脑GnRH脉冲式释放决定的。用青春期前的幼猴实验表明,破坏产生GnRH的弓状核后, 连续滴注外源的GnRH并不能诱发青春期的出现,只有按照内源GnRH所表现的脉冲式频率和幅度滴注GnRH,才能使 血中LH与FSH浓度呈现类似正常的脉冲式波动,从而激发青春期发育。看来,激素呈脉冲式释放对发挥其作用是十分重要的。
腺垂体的促性腺激素细胞的膜上有GnRH受体,GnRH与其受体结合后,可能是通过磷脂酰肌醇信息传递系统导致细胞内Ca2+浓度增加而发挥作用的。
在人的下丘脑,GnRH主要集中在弓状核、内侧视前区与室旁核。除下丘脑外,在脑的其他区域如间脑、边缘叶,以及松果体、卵巢、睾丸、胎盘等组织中,也存在着GnRH。GnRH对性腺的直接作用则是抑制性的,特别是药理剂理的GnRH,其抑制作用更为明显,对卵巢可抑制卵泡发育和排卵,使雌激素与孕激素生成减少;对睾丸则抑制精子的生成,使睾酮的分泌减低。
(三)生长抑素与生长素释放激素
1.生长抑素(生长素释放抑制素,growth hormone release-inlease-inhibiting hormone,GHRIH,或somatostatin)是由116个氨基酸的大分子肽裂解而来的十四肽,其分了结构呈环状,在第3位和第14位半胱氨酸之间有一个二硫键。生长抑素是作用比较广泛的一种神经激素,它的主要作用是抑制垂体生长素(GH)的基础分泌,也抑制腺垂体对多种刺激所引起的GH分泌反应,包括运动、进餐、应激、低血糖等。另外,生长抑素还可抑制LH、FSH、TSH、PRL及 ACTH的分泌。生长抑素与腺垂体生长素细胞的膜受体结合后,通过减少细胞内cAMP和 Ca2+而发挥作用。
除下丘脑外,其他部位如大脑皮层、纹状体、杏仁核、海马,以及脊髓、交感神经、胃肠、胰岛、肾、甲状腺与甲状旁腺等组织广泛存在生长抑素。在脑与胃肠又纯化出28个氨基酸组成的在GHRIH28,它是GHRIH14N端向外延伸而成。生长抑素的垂体外作用比较复杂,它在神经系统可能起递质或调质的作用;生长抑素对胃肠运动与消化道激素的分泌均有一定的抑制作用;它还抑制胰岛素、胰高血糖素、肾素、甲状旁腺激素以及降钙素的分泌。
2.生长素释放激素(growth hormone releasing hormone,GHRHA)由于下丘脑中GHRH的含量极少,致化学提取困难。1982年有人首先从一例患胰腺癌伴发肢端肥大症患者的癌组织中提取并纯化出一种44个氨基酸的肽,它在整体和离体实验均显示有促GH分泌的生物活性。1983年,从大鼠下丘脑中提纯了GHRH43,这种四十三肽对人的腺垂体也有很强有促GH分泌作用。近年用DNA重组扶得到GHRH40和GHRH44的基因,这些基因已被克隆化,并非酵母系统中传代和表达,为提供充足与兼价的GHRH开拓了可喜的前景。
产生GHRH的神经元主要分布在下丘脑弓状核及腹内侧核,它们的轴突投射到正中隆起,终止于垂体门脉初级毛细血管旁。GHRH呈脉冲式释放,从而导致腺垂体的GH分泌也呈现脉冲式。大鼠实验证明,注射GHRH抗体后,可消除血中GH浓度的脉冲式波动。一般认为,GHRH是GH分泌的经常性调节者,而GHRIH则是在应激刺激GH分泌过多时,才显著地发挥对GH分泌的抑制作用。GHRH与GHRIH相互配合,共同调节腺垂体GH的分泌。
在腺垂体生长素细胞的膜上有GHRH受体,GHRH与其受体结合后,通过增加内cAMP与Ca2+促进GH释放。
(四)促肾上腺皮质激素释放激素
促肾上腺皮质激素释放激素(corticotropin releasing hormone,CRH)为四十一肽,其主要作用是促进腺垂体合成与释放促肾上腺皮质激素(ACTH)。腺垂体中存在大分子的促阿片-黑素细胞皮质素原(pro-opiomelanocortin,POMC),简称阿黑皮素原。在CRHA作用下经酶分解了ACTH、溶脂激素(lipotropin,β-LPH)和少量的β-内啡肽。静脉注射CRH5-20min后,血中ACTH浓度增加5-20倍。
分泌CRH的神经元主要分布在下丘脑室旁核,其轴突多投射到正中隆起。在下丘脑以外部位,如杏仁核、海马、中脑,以及松果体、胃肠、胰腺、肾上腺、胎盘等处组织中,均发现有CRH存在。下丘脑CRH以脉冲式释放,并呈现昼夜周期节律,其释放量在6-8点钟达高峰,在0点最低。这与ACTH及皮质醇的分泌节律同步。机体遇到 的应激刺激,如低血溏、失血、剧痛以及精神紧张等,作用于神经系统不同部位,最后将信息汇集于下丘脑CRH神经元,然后通过CRH引起垂体-肾上腺皮质系统反应。
CRH与腺垂体促肾上腺皮质激素细胞的膜上CRH受体结合,通过增加细胞内cAMP与Ca2+促进ACTH的释放。
(五)催乳素释放抑制因子与催乳素释放因子
下丘脑对腺垂体催乳素(PRL)的分泌有抑制和促进两种作用,但平时以抑制作用为主。首先在哺乳动物下丘脑提取液中,发现一种可抑制腺垂体释放PRL的物质,称为催乳素释放抑制因子(prolactin release-inhibiting factor,PIF)。随后,又在下丘脑提取液中发现还有一咱能促进腺垂体释放PRL的因子,称为催乳素释放因子(prolactin releasing factor,PRF)。将下丘脑提取液中的TRH分离出去,仍具有PRF活性,说明下丘脑提取液中PRF活性不是来自TRH。PIF与 PRF的化学结构尚不清楚,由于多巴肽可直接抑制腺垂体PRL分泌,注射多巴胺可使正常人或高催乳素血症患者血中的PRL明显下降,而且在下丘脑和垂体存在的多巴胺,因此有人进出多巴胺可能就是PIF的观点。
(六)促黑素细胞激素释放因子与抑制因
促黑素细胞激素释放因子(melanophore-stimulating hormone releasing factor,MRF)(melanophore-stimulating hormone release-inhibiting factor,MIF)可能是催产素裂解出来的两种小分子肽。MRF促进MSH的释放,而MIF则抑制MSH的释放。
二、调节下丘脑肽能神经元活动的递质
下丘脑能神经元与来自其他部位的神经纤维有广泛的突触联系,其神经递质比较复杂,可分为两大类:一类递质是肽类物质,如脑啡肽、β-内啡肽、神经降压素、P物质、血管活性肠肽及胆囊收缩素等;另一类递质是单胺类物质,主要有多巴胺(DA)、去甲肾上腺素(NE)与 5-羟色胺(5-HT)。
组织化学研究表明,三种单受类递质的浓度,以下丘脑“促垂体区”正中隆起附近最高。单胺能神经元可直接与释放下丘脑调节肽的肽能神经元发生突触联系,也可以通过多突触发生联系。单胺能神经元通过释放单胺类递质,调节肽能神经元的活动。下丘脑单受能神经元的活动不断受中枢神经系统其他部位的影响,所以它们对下丘脑调节肽分泌的调节作用比较复杂。
近年来的研究表明,阿片肽对下丘脑调节肽的释放有明显的影响。例如,给人注射脑啡肽或β-内啡肽可抑制CRH的释放,从布使ACTH分泌减少,而纳洛酮则有促进CRH释放的作用;注射脑啡肽或β-内啡肽可刺激下丘脑释放TRH和GHRH,使腺垂体分泌TSH与GH增加,而对下丘脑的 GnRH释放则明显的抑制作用。
垂体按其胚胎发育和功能、形态的不同,分为腺垂体和神经垂体两部分。腺垂体来自胚胎口凹的外胚层上皮,是由6种腺细胞组成的上皮细胞。神经垂体来自间脑底部的漏斗,主要由下丘脑-垂体束的无髓神经纤维和神经胶质细胞分化而成的神经垂体细胞组成。垂体以漏斗与下丘脑相连。由于在形成与功能上下丘脑与垂体的联系非常密切,可将它们看作一个功能单位。
一、腺垂体
腺垂体是体内最重要 的内分泌腺。它由不同的腺细胞分泌七种激素:由生长素细胞分泌生长素(GH);由促甲状腺激素细胞分泌促甲状腺激素(TSH);由促肾上腺皮质激素细胞分泌促肾上腺皮质激素(ACTH)与促黑(素细胞)激素(MSH);由促性腺激素细胞分泌卵泡刺激素(FSH)与共同体生成素(LH);由催乳素细胞分泌催乳素(PRL)。在腺垂体分泌的激素中,TSH、ACTH、FSH与LH均有各自的靶腺,分别形成: ①下丘脑-垂体-甲状腺轴;②下丘脑-垂体-肾上腺皮质轴;③下丘脑-垂体-性腺轴。腺垂体的这些激素是通过调节靶腺的活动而发挥作用的,而GH、PRL与MSH则不通过靶腺,分别直接调节个体生长、乳 腺发育与泌乳、黑素细胞活动等。所以,腺垂体激素的作用极为广泛而复杂。
(一)生长素
人生长素(human growth hormone,hGH)含有191个氨基酸,分子量为22000,其化学结构与会催乳素近似,故生长素有弱催乳素作用,而催乳素有弱生长素作用。不同种类动物的生长素,其化学结构与免疫性质等有较大差别,除猴的生长素外,其他动物的生长素对人无效。近年利用DNA重组技术可以大量生产hGH,供临床应用。人GH的化学结构见图11-6。
1.生长素的作用 GH的生理作用是促进物质代谢与生长发育,对机体各个器官与各种组织均有影响,尤其是骨骼、肌肉及内脏器官的作用更为显著,因此,GH也称为躯体刺激素(somatotropin)。
(1)促进生长作用:机体生长受多种激素的影响,而GH是起关键作用的调节因素。幼年动物摘除垂体后,生长即停止,如及时补充GH则可使其生长恢复。人幼年时期GH,将出现生长停滞,身材矮小,称为侏儒症;如GH过多则患巨人症。人成年后GH过多,由于长骨骨骺已经钙化,长骨不再生长,只能使软骨成分较多的手脚肢端短骨、面骨及其软组织生长异常,以致出现手足粗大、鼻大唇厚、下颌突出等症状,称为肢端肥大症。正常成年男子在空腹安静状态下,血浆中GH浓度不超过5μg/L,成年女子不超过10μg/L。而巨人症与肢端肥大症患者血中GH浓度可明显增高。
GH的促生长作用是由于它能促进骨、软骨、肌肉以及其他组织细胞分裂增殖,蛋白质合成增加,离体软骨培养实验发现,将GH加入到去垂体动物的软骨培养液中,对软骨的生长无效,而加入正常动物的血浆却有效,说明GH对软骨的生长并无直接作用,而在正常动物血浆中存在某种有促进生长作用的因子。实验研究证明,GH主要诱导肝产生一种具有促生长作用的肽类物质,称为生长介素(somatomedin,SM),因其化学结构与胰岛素看近似,所以又称为胰岛素样生长因子(insulin-like growth factor,IGF)。目前已分离出两种生长介素,即IGF-I和IGF-Ⅱ,它们分子组成的氨基酸有70%是相同的。IGF-I是含有70个氨基酸的多肽,GH的促生长作用主要是通过IGF-I作介导的。IGF-Ⅱ是含有67个氨基酸的多肽,它主要在胚胎期产生,对胎儿的生长起重要作用。血液中的IGF-I含量信号2于GH的水平,摘除垂体的大鼠血中IGF-I含量降低,注射GH后,血中IGF-I含量增加,并与GH的剂量呈依赖式。活动期肢端肥大症患者血中IGF-I含量明显增高而侏儒症患者血中IGF-I含量明显低于正常。给人注射GH,往往需要12-18h后,血中IGF-I含量才会升高,所以当血中GH浓度有急剧变化时,在一定时间内血中IGF-I的含量可维持相对稳定,在青春期,随着GH分泌增多,血中IGF-I的浓度也相应增加。
给幼年动物注射生长介素能明显刺激动物生长,身长增高,体重增加,IGF-Ⅱ比IGF-I的促生长作用更强。生长介素主要的作用是促进软骨生长,它除了可促进硫酸盐进入软髓组织外,还促进氨基酸进入软骨细胞,增强DNA、RNA和蛋白质的合成,促进软骨组织增殖与骨化,使长骨加长。
血中的生长介素,绝大部分与生长介素结合蛋白结合,被运送到全身各处除肝外,肌肉、肾、心与肺等组织也能产生生长介素,可能以旁分泌的方式,以局部起作用。
(2)促进代谢作用:GH可通过生长介素促进氨基酸进入细胞,加速蛋白质合成,包括软骨、骨、肌肉、肝、肾、心、肺、肠、脑以皮肤等组织的蛋白质合成增强;GH促进脂肪分解,增强脂肪酸氧化,抑制外周组织摄取与利用葡萄糖,减少葡萄糖的消耗,提高血糖水平。GH对脂肪与糖代谢的作用似乎与生长介素无关,机制尚不清楚。
近年研究证明,血中的生长介互可对GH分泌有负反馈调节作用。IGF-I能刺激下丘脑释放GHRIH,从而抑制GH的分泌。IGF-I还能直接抑制培养的腺垂体细胞GH的基础分泌和GHRH刺激的GH分泌,说明IGF-I可通过下丘脑和垂体两下水平对GH分泌进入负反馈调节。
除了上述的调控机制外,还有许多因素可以影响GH的分泌:
(1)睡眠的影响:人在觉醒状态下,GH分泌较少,进入慢波睡眠后,GH分泌明显增加,约在60min左右,血中GH浓度达到高峰。转入异相睡眠后,GH分泌又减少。看来,在慢波睡眠其GH分泌增多,对促进生长和体力恢复是有利的。50岁以后,GH这种分泌峰 消失。
(2)代谢因素的影响:血中糖、氨基酸与脂肪酸均能影响GH的分泌,其中以低血糖对GH分泌的刺激作用最强。当静脉注射胰岛素使血糖降至500mg/L以下时,经30-60min,血中GH浓度增加2-10倍。相反,血糖升高可使GH浓度降低。有人认为,在血糖降低时,下丘脑GHRH神经元兴奋性提高,释放GHRH增多,GH分泌增加,可减少外周组织对葡萄糖的利用,而脑组织对葡萄糖的利用可基本不受影响。血中氨基酸与脂肪酸增多可引起GH分泌增加,有利于机体对这些物质的代谢与利用。
此外,运动、应激刺激、甲状腺激素、雌激素与睾酮无法能促进GH分泌。在青春其,血中雌激素或睾酮浓度增高,可明显地增加GH分泌,这是在期GH分泌较多的一个重要因素。
(二)催乳素
催乳素(prolactin,PRL)是含199个氨基酸并有三个二硫键的多肽,分子量为22000。在血中还存在着较大分子的PRL,可能是PRL的前体或几个PRLA分子 的聚合体,成人血浆中的PRL浓度<20μg/L。
PRL的作用极为广泛,下面仅就其主要作用加以扼要说明。
1.对乳腺的作用 PRL引起并维持泌乳,故名催乳素。在女性青春期乳腺的发育中,雌激素、孕激素、生长素、皮质醇、胰岛素、甲状腺激素及PRL起着重要的作用。到妊娠期,PRL、雌激素与孕激素分泌增多,使乳腺组织进一步发育,具备泌乳能力却不泌乳,原因是此时血中雌激素与孕激素浓度过高,抑制PRL的泌乳作用。分娩后,血中的雌激素和孕激素浓度大大降低,PRL才能地发挥始动和维持泌乳的作用。在妊娠期PRL的分泌显著增加,可能与雌激素刺激垂体催乳素细胞的分泌活动有关。妇女授乳时,婴儿吸吮乳头反射性引起PRL大量分泌。
2.对性腺的作用 在哺乳类运物,PRL对卵巢的黄体功能有一定的作用,如啮齿类,PRL与LH配合,促进黄体形成并维持分泌孕激素,但大剂量的PRL又能使黄体溶解。PRL对人类的卵巢功能也有一定的影响,随着卵泡的发育成熟,卵泡内的PRL含量逐渐增加,并在次级留言簿包发育成为排卵前卵泡的过程中,在颗粒细胞上出现PRL受体,它是在FSH的刺激下形成的。PRL与其受体结合,可刺激LH受体生成,LH与其受体结合后,促进排卵、黄体生成及孕激素与雌激素的分泌。实验表明,小量的PRL对卵巢激素与孕激素的合成起允许作用,而大量的PRL则有抑制作用。临床上患闭经溢乳综合症的妇女,表现特征为闭经、溢乳与不孕,患者一般都存在无排卵与雌激素水平低落,而血中PRL浓度却异常增高。
男性在睾酮存在的条件下,PRL促进前列腺及精囊腺的生长,还可以增强LH对间质细胞的应用,使睾酮的合成增加。
PRL参与反激反应。 在应激状态下,血中PRL浓度升高,而且往往与ACTH和GH浓度的增高一出现,刺激停止数小时后才逐渐恢复到正常水平。看来,PRL可能与ACTH及GH一样,是应激反应中腺垂体分泌的三大激素之一。
腺垂体PRL的分泌受下丘脑PRF与PIF的双重控制,前者促进PRL分泌,而执行者则抑制其分泌。多巴胺通过下丘脑或直接对腺垂体PRL分泌有抑制作用。下丘脑的TRH能促进PRL的分泌。吸吮乳头的刺激引起传入神经冲动,经脊髓上传至下丘脑,使PRF神经元发生兴奋,PRF释放增多,促使腺垂体分泌PRL增加,这是一个典型的神经内分泌反射。
二、神经垂体
神经垂体不含腺体细胞,不能合成激素。所谓的神经垂体激素是指在下丘脑视上核、室旁核产生而贮存于神经垂体的升压素(抗利尿激素)与催产素,在适宜的刺激作用下,这两种激素由神经垂体释放进入血液循环。
升压素(vasopressin, VP或antidiuretic hormone,ADH)与催产素(oxytocin,OXT)在下丘脑的视上核与室旁核均可产生,但前者主要在视上核产生,而后者主要在室旁核产生。它们的化学结构都是九肽,催产素与升压素只是第3位与第8位的氨基酸残基有所不同。人升压素的第8位氨基酸为精氨酸,故称为精氨酸升压不比(arginine vasopressin,AVP)。这两种激素已能人工合成。
实验证明,升压素与催产素是在视上核和室旁核神经元的核蛋白体上先形成激素有前身物质(激素原) ,再裂解成神经垂体激素的,并与同时合成的神经垂体激素运载蛋白(neurophysin)形成复合物,包装于囊泡中,呈小颗粒状。在轴突内,囊泡以每天2-3mm的速度运送至神经垂体。在适宜刺激的作用下,视上核或室旁核发生兴奋,神经冲动将沿着下丘脑-垂体束传导至神经垂体中的神经末梢,使其发生去极化,导致Ca2+内流进入末梢内,促进末梢的分泌囊泡经出泡作用而将神经垂体激素与其运载蛋白一并释放进入血液。
神经垂体激素运载蛋白有两种:一种与催产素结合释放入血液的,称为运载蛋白I,由92个氨基酸组成;另一种与升压素结合的称为运载蛋白Ⅱ,由97个氨基酸组成,烟碱可使血浆中运载蛋白Ⅱ和升压素浓度同时升高,而雌激素可使血浆中运载蛋白I含量增加,而催产素浓度并不随之增加。
有资料表明,神经垂体激素不仅存在于下丘脑-垂体束系统内,而且在下丘脑正中隆起与第三脑室附近的神经元轴突中也有神经垂体激素。在大鼠和猴的垂体门脉血液中,检测出大量的升压素,其浓度远远主于外周血液中的浓度,而且注射大量的升压素能引起腺垂体ACTH分泌增加,提示神经垂体激素可能影响垂体的分泌活动。
(一)升压素(抗利尿激素)
血浆中升压素浓度为1.0-1.5ng/L,它在血浆中的半衰期仅为6-10mim。升压素的生理浓度很低,几乎没有收缩血管而致血压升高的作用,对正常血压调节没有重要性,但在失血情况下由于升压素释放较多,对维持血压有一定的作用。但是,升压素的抗利尿作用却十分明显,因此称为抗利尿激素较为适宜。
关于抗利尿激素的作用与分泌的调节,在第四章和第八章已有详细叙述。
(二)催产素
催产素具有促进乳汁排出一刺激子宫收缩的作用。
1.对乳腺的作用 哺乳期乳腺不断分泌乳汁,贮存于腺泡中,当腺泡周围具有收缩性的肌上皮细胞时,腺泡压力增高,使乳汁从腺泡经输乳管由乳头射出。射乳是一典型的神经内分泌反射。乳头含有丰富的感觉神经末梢,吸吮乳头的感觉信息经传入神经传至下丘脑,使分泌催产素的神经元发生兴奋,神经冲动经下丘脑-垂体束传送到神经垂体,使贮存的催产素释放入血,并作用于乳腺中的肌上皮细胞使之产生收缩,引起乳汁排出,在射乳反射过程 ,血中抗利尿激素浓度毫无变化。在射乳反射的基础上,很容易建立条件反射,如母亲见到婴儿或听到其哭声均可引起条件反向性射乳。催产素除引起乳汁排出外,还有维持哺乳期乳腺不致萎缩的作用。
在射乳反射中,催乳素与催产素的分泌一同增加,而GnRH的释放减少。催乳素分泌增多促使GnRH分泌,对下一次射乳有利。GnRH释放减少引起腺垂体促性腺激素分泌减低,可导致哺乳期月经暂停。GnRH释放减少可能由于吸吮乳头刺激引起下丘脑多巴胺神经元兴奋,释放多巴胺,多巴胺可抑制GnRH的释放;也可能与下丘脑的β-内啡肽有关。它既可促进催乳素分泌,又可抑制GnRH的释放。
2.以子宫的作用 催产素促进子宫肌收缩,但此种信息处理民子宫的功能状态有关。催产素对非孕子宫的作用较弱,而对妊娠子宫的作用较强,雌激素能增加子宫对催产素的敏感性,而孕激素则相反,催产素可使细胞外Ca2+进入子宫平滑肌细胞内,提高肌细胞内的Ca2+浓度,可能通过钙调蛋白的作用,并在蛋白激酶的参与下,诱发肌细胞收缩。研究表现,催产素虽然刺激子宫收缩,但它并不是发动分娩子宫进一步收缩。
由于催产素与抗利尿激素的化学结构相似,它们的生理作用有一定程度的交叉,例如,催产素对犬的抗利尿作用相当于抗利尿激素的1/200,而抗利尿激素对大鼠离体子宫的收缩作用为催产素的1/500左右。
甲状腺是人体内最大的内分泌腺,平均生理约为20-25g。甲状腺内含有许多大小不等的圆形或椭圆形腺泡。腺泡是由单层的上皮细胞围成,腺泡腔内充满胶质。胶质是腺泡上皮细胞的分泌物,主要成分为甲状腺球蛋白。腺泡上皮细胞是甲状腺激素的合成与释放的部位,而腺泡腔的胶质是激素有贮存库。腺泡上皮细胞的形态物质及胶质的量随甲状腺功能形态的不岢发生相应的变化。腺泡上皮细胞通常为立方形,当甲状腺受到刺激而功能活跃时,细胞变高呈低柱状,胶质减少;反之,细胞变低呈扁平形,而胶质增多。
在甲状腺腺泡之间和腺泡上皮细胞之间有滤泡旁细胞,又称C细胞,分泌降钙素。
一、甲状腺激素的合成与代谢
甲状腺激素主要有甲状腺素,又称甲碘甲腺原氨酸(thyroxine,3,5,3’,5’-tetraiodotyyronine,T4)和三碘甲腺原氨酸(3,5,3’-triiodothyronine,T3)两种,它们都是酷氨酸碘化物。另外,甲状腺也可合成极少量的逆-T3(3,3’,5’-T3或reverse T3,rT3),它不具有甲状腺激素有生物活性。
甲状腺激素合成的原料有碘和甲状腺球蛋白,在甲状腺球蛋白的酪氨酸残基上发生碘化,并合成甲状腺激素。人每天从食物中大约摄碘100-200μɡ,占合身碘量的90%。因此,甲状腺与碘代谢的关系极为密切。
在胚胎期11-12周,胎儿甲状腺开始有合成甲状腺激素的能力,到13-14周在胎儿垂体促甲状腺激素的刺激下,甲状腺加强激素的分泌,这对胎儿脑的发育起着关键作用,因为母体的甲状腺激素进入胎儿体内的量很少。
甲状腺激素的合成过程包括三步:
(一)甲状腺腺泡聚碘
由肠吸收的碘,以I-形式存在于血液中,浓度为250μg/L,而μg/L内I-浓度比血液高20-25倍,加上甲状腺上皮细胞膜静息电位为-50mV,因此,I-从血液转运进入甲状腺上皮细胞内,必须逆着电化学梯度面进行主动转运,并消耗能量。在甲状腺腺泡上皮细胞在底面的膜上,可能存在I-转运蛋白,它依赖Na+-K+-ATP酶活动提供能量来完全I-的主动转运,因为用哇巴因抑制ATP酶,则聚碘作用立即发生障碍。有一些离子,如过氯酸盐的COO4-、硫氰桎卤的SCN-GN I-竞争转运机制,因此能抑制甲状腺的聚碘作用。摘除垂体可降低聚碘能力,而给予TSH则促进聚碘。用同位素(Na131I)示踪法观察甲状腺对放射性碘的摄取,在正常情况下有20%-30%的碘被甲状腺摄取,临床常用摄取放射性碘的能力来检查与判断甲状腺的功能状态。
(二)I-的活化
摄入腺泡上皮细胞的I-,在过氧化酶的作用下被活化,活化的部位在腺泡上皮细胞项端质膜微绒毛与腺泡腔交界处。活化过程的本质,尚未确定,可能是由I-变成I2或I0。或是与过氧化酶形成某种复合物。
I-的活化是碘得以取代酪氨酸残基上氢原子的先决条件。如先天缺乏过剩,I-不以活化,将使甲状腺激素有合成发生障碍。
(三)酷氨酸碘化与甲状腺激素的合成
在腺泡上皮细胞粗面内质网的核糖体上,可形成一种由四个肽链组成的大分子糖蛋白,即甲状腺球蛋白(thyroglobulin,TG),其分子量为670000,有3%的酪氨酸残基。碘化过程就是发生在甲状腺球蛋白的酪氨酸残基上,10%的酪氨酸残基可被碘化。放射自显影实验证明,注入放射性碘几分钟后,即可在甲状腺腺泡上皮细胞微绒毛与腺泡腔壁的上皮细胞残部,即能碘化甲状腺球蛋白,说明碘化过程发生在甲状腺腺泡上皮细胞微绒毛与腺泡交界处。
甲状腺球蛋白酪氨酸残基上的氢原子可被碘原子取代或碘化,首先生成一碘酪氨酸残基(MIT)和二碘酪氨残基(DIT),然后两个分子的DIT耦联生成四碘甲腺原氨酸(T4);一个分子的MIT与一个分子的DIT发生耦联,形成三碘甲腺原氨酸(T3),还能合成极少量的rT3。
上述酪氨酸的碘化和碘化酪氨酸的耦联作用,都是在甲状腺球蛋白的分子上进行的,所在甲状腺球蛋白的分子上既含有酪氨酸、碘化酪氨酸,也常含有MIT、DIT和T4及T3。在一个甲状腺球蛋白分子上,T4与T3之比为20:1,这种比值常受碘含量的影响,当甲状腺内碘化活动增强时,DIT增多,T4含量也相应增加,在缺碘时,MIT增多,则T3含量明显增加。
甲状腺过氧化酶是由腺上皮细胞的核糖体生成的,它是一种含铁卟啉的蛋白质,分子量为60000-100000,在腺上皮顶缘的微绒毛处分布最多。实验证明,甲状腺过氧化酶的活性受TSH的调控,大鼠摘除垂体48h后,甲状腺过氧化酶活性消失,注入TSH后此酶活性再现。甲状腺过氧化酶的作用是促进碘活化、酪氨酸残基碘化及碘化酪氨酸的耦联等,所以,甲状腺过氧化酶晨甲状腺激素的合成过程中起关键作用,抑制此酶活性的药物,如硫尿嘧啶,便可抑制甲状腺激素的合成,可用于治疗甲状腺功能亢进。
(四)甲状腺激素有贮存、释放、运输与代谢
1.贮存 在甲状腺球蛋白上形成的甲状腺激素,在腺泡腔内以胶质的形式贮存。甲状腺激素有贮存有两个特点:一是贮存于细胞外(腺泡腔内);二是贮存的量很大,可供机体利用50-120天之久,在激素贮存的量上居首位,所以应用抗甲状腺药物时,用药时间需要较长才能奏效。
2.释放 当甲状腺受到TSH刺激后,腺泡细胞顶端即活跃起来,伸出伪足,将含有T4、T3及其他多种碘化酪酸残基的甲状腺球蛋白胶质小滴,通过吞饮作用,吞入腺细胞内(图11-9)。吞入的甲状腺球蛋白随即与溶酶体融合而形成吞噬体,并在溶酶体蛋白水解酶的作用下,将T4、T3以及MIT和DIT水解下来。甲状腺球蛋白分子较大,一般不易进入血液循环,而MIT和DIT的分子虽然较小,但很快受脱 碘酶的作用而脱碘,脱下来的碘大部分贮存在甲状腺内,供重新利用合成激素,另一小部分从腺泡上皮细胞释出,进入 血液。T4和T3对腺泡上皮细胞内的脱碘不敏感,可迅速进入血液。此外,尚有微量的rT3、MIT和DIT也可从甲状腺释放,进入血中。已经脱掉T4、T3、MIT和DIT的甲状腺球蛋白,则被溶酶体中的蛋白水解酶所水解。
由于甲状腺球蛋白分子上的T4数量远远超过T3,因此甲状腺分泌的激素主要是T4,约占总量的90%以上,T3的分泌量较少,但T3的生物活性比T4约大5倍
3.运输 T4与T3释放入血之后,以两种形式在血液中运输,一种是与血浆蛋白结合,另一种则呈游离状态,两者之间可互相转化,维持动态平衡。游离的甲状腺激素在血液中含量甚少,然而正是这些游离的激素才能进入细胞发挥作用,结合型的甲状腺激素是没有生物活性的。能与甲状腺激素结合的血浆蛋白有三种:甲状腺素结合球蛋白(thyroxine-binding globulin,TBG)、甲状腺素结合前白蛋白(thyroxine-binding prealbumin,TBPA)与白蛋白。它们可与T4和T3发生不同程度的结合。血液中T4有99.8%是与蛋白质结合,其余10%与白蛋白结合。血中T4与TBG的结合受TBG含量与T4含量变化的影响,TBG在血浆听浓度为10mg/L,可以结合T4100-260μg。T3与各种蛋白的亲和力小得多,主要与TBG结合,但也只有T4结合量的3%。所以,T3主要以游离形式存在。正常成年人血清T4浓度为51-142nmol/L,T3浓度为1.2-3.4nmol/L。
4.代谢 血浆T4半衰期为7天,半衰期为1.5天,20%的T4与T3在肝内降解,也葡萄糖醛酸或硫酸结合后,经胆汁排入小肠,在小肠内重吸收极少,绝大部分被小肠液进一步分解,随粪排出。其余80%的T4在外周组织脱碘酶(5’- 脱碘酶或5-脱碘酶)的作用下,产生T3(占45%)与rT3(占55%)。T4脱碘变成T3是T3的主要来源,血液中的T3有75%来自T4,其余来自甲状腺;rT3仅有少量由甲状腺分泌,绝大部分是在组织内由T4脱碘而来。由于T3的作用比T4大5倍,所以脱碘酶的活性将影响T4在组织内发挥作用,如T4浓度减少可使T4转化为T3增加,而使rT3减少。另外妊娠、饥饿、应激、代谢紊乱、肝疾病、肾功能衰竭等均会使T4转化为rT3增多。T3或rT3可再经脱碘变成二碘、一碘以及不含碘的甲状腺氨酸。另外,还有少量的T4与T3在肝和肾组织脱氨基和羧基,分别形成四碘甲状腺醋酸与在三碘甲状腺醋酸,并随尿排出体外。
二、甲状腺激素的生物学作用
T4与T3都具有生理作用。由于T4在外周组织中可转化为T3,而且T3的活性较大,曾使人认为T4可能是T3激素原,T4只有通过T3才有作用。目前认为,T4不仅可作为T3的激素原,而且其本身也具有激素作用,约占全部甲状腺激素作用的35%左右。临床观察发现,部分甲状腺功能低下患者的血中T3浓度强;另外,实验证明,在甲状腺激素作用的细胞核受体上,既存在T3结合位点,也有T4结合位点,T3或T4与其结合位点的亲和力是不同的,T3比T4高10倍。这些资料提示,T4本身也具有激素作用。
甲状腺激素的主要作用是促进物质与能量代谢,促进生长和发育过程。机体未完全分化与已分化的组织,对甲状腺激素的反应可以不同,而成年后,不同的组织对甲状腺的敏感性也有差别。甲状腺激素除了与核受体结合,影响转录过程外,在核糖体、线粒体、以及细胞膜上也发现了它的结合位点,可能对转录后的过程、线粒体的生物氧化作用以及膜的转运功能均有影响,所以,甲状腺激素的作用机制十分复杂。
(一)对代谢的影响
1.产热效应 甲状腺激素可提高绝大多数组织有耗氧率,增加产热量。有人估计,1mgT4可使组织产热增加,提高基础代谢率28%。给动物注射甲状腺激素后,需要经过一段较长时间的潜伏期才能出现生热作用。T4为24-48h,而T3为18-36h,T3的生热作用比T4强3-5倍,但持续时间较短。给动物注射T4或T3后,取出各种组织进入离体实验表明,心、肝、骨骼肌和肾等组织耗氧率明显增加,但另一些组织,如脑、肺、性腺、脾、淋巴结和皮肤等组织的耗氧率则不受影响。在胚胎期胎儿大脑组织可受甲状腺激素的作用而增加耗氧率,但出生后,大脑组织就失去了这种反应能力。
近年的研究表明,动物注射甲状腺激素后,心、肝、肾和骨骼肌等组织出现产热效应时,Na+-K+-ATP酶活性明显升高,如用哇巴因抑制此酶活性,则甲状腺激素的产热效应可完全被消除。又如,甲状腺功能低下的大鼠,血中甲状腺激素含量下降,其肾组织细胞膜Na+-K+-ATP酶活性减弱,若给予T4,酶的活性可恢复甚至增加,由此看来,甲状腺激素的产热作用与Na+-K+-ATP酶的关系十分 密切。另外,有 人认为,甲状腺激素也能促进脂肪酸氧化,产生大量的热能。
甲状腺功能亢进时,产热量增加,基础代谢率升主患者喜凉怕热,极易出汗;而甲状腺功能低下时,产热量减少,基础代谢率降低,患者喜热恶寒,两种情况无法不能适应环境温度的变化。
2.对蛋白质、糖 和脂肪代谢的影响
(1)蛋白质代谢:T4或T3作用于核受体,刺激DNA转录过程,促进mRNA形成,加速蛋白质与各种酶的生成。肌肉、肝与肾的蛋白质合成明显增加,细胞数量增多,体积增大,尿氮减少,表现为正氮平衡。甲状腺激素分泌不足时,蛋白质合成减少,肌肉收缩无力,但组织间的粘蛋白增多,可结合大量的正离子和水分子,引起粘液性水肿(myxedema)。甲状腺分泌过多时,则加速蛋白质分解,特别是促进骨骼蛋白质分解,使肌酐含量降低,肌肉收缩元力,尿酸含量增加,并可促进骨的蛋白质分解,从而导致血钙升高和骨质疏松,尿钙的排出量增加。
(2)糖代谢:甲状腺激素促进小肠粘膜对糖的吸收,增强糖原分解,抑制糖原合成,并能增强肾上腺素、胰高血糖素、皮质醇和生长素的生糖作用,因此,甲状腺激素有升主血糖的趋势;但是,由于T4与T3还可加强外周组织对糖的利用,也有降低血糖的作用。甲状腺功能亢进时,血糖常升高,有时出现糖尿。
(3)脂肪代谢:甲状腺激素促进脂肪酸氧化,增强儿茶酚胺与胰高血糖素对脂肪的分解作用。T4与T3既促进胆固醇的合成,又可通过肝加速胆固醇的降解,而且分解的速度超过合成。所以,甲状腺功能亢进患者血中胆固醇含量低于正常。
甲状腺功能亢进时,由于蛋白质、糖和脂肪的分解代谢增强,所以患者常感饥饿,食欲旺盛,且有明显消瘦。
(二)对生成与发育的影响
甲状腺激素具有促进组织分化、生长与发育成熟的作用。切除甲状腺的蝌蚪,生长与发育停滞,不能变态成蛙,若及时给予甲状腺激素,又可恢复生长发育,包括长出肢体、尾巴消失,躯体长大,发育成蛙。在人类和哺乳动物,甲状腺激素是维持正常生长也发育不可缺少的激素,特别是对骨和脑的发育尢为重要。甲状腺功能低下的儿童,表现为以智力迟钝生身体矮小为特征的呆小症(又称克汀病)。在胚胎期缺碘造成甲状腺激素合成不足,或出生后甲状腺功能低下,脑的发育明显障碍,脑各部位的神经细胞变小,轴突、树突与髓鞘均减少,胶质细胞数量也减少。神经组织内的蛋白质、磷脂以及各种重要的酶与递质的含量都减低。甲状腺激素刺激骨化中心发育,软骨骨化,促进长骨和牙齿的生长。值得提出的是,在胚胎期胎儿骨的生长并不必需甲状腺激素,所以患先天性甲状腺发育不全的胎儿,出生后身长可以基本正常,但脑的发育已经受到程度不同的影响。在出生后数周至3-4个月后,就会表现出明显的智力迟钝和长骨生长停滞。所以,在缺碘地区预防呆小症的发生,应在妊娠期注意补充碘,治疗呆小症必须抓时机,应在生后三个月以前补给甲状腺激素,过迟难以奏效。
(三)对神经系统的影响
甲状腺激素不但影响中枢系统的发育,对已分化成熟的神经系统活动也有作用。甲状腺功能亢进时,中枢神经系统的兴奋性增高主要表现为注意力不易集中、过敏疑虑多愁善感、喜怒失常、烦躁不安、睡眠不好而且多梦幻,以及肌肉纤颤等。相反,甲状腺功能低下时,中枢神经系统兴奋性降低,出现记忆力减退,说话和行动迟缓,淡漠无怀与终日思睡状态。
甲状腺激素除了影响中枢神经系统活动外,也能兴奋交感神经系统,其作用机制还不十分清楚。
另外,甲状腺激素对心脏的活动有明显影响。T4与T3可使心率增快,心缩力增强,心输出量与心作功增加。甲状腺功能亢进患者心动过速,心肌可因过度耗竭而致心力衰竭。离体培养的心细胞实验表明,甲状腺激素可直接作用于心肌,T3能增加心肌细胞膜上β受体的数量,促进肾上腺素刺激心肌细胞内cAMP的生成。甲状腺激素促进心肌细胞肌质网释放Ca2+,从而激活与心肌收缩有关的蛋白质,增强收缩力。
三、甲状腺功能的调节
甲状腺功能活动主要受下丘脑与垂体的调节。下丘脑、垂体和甲状腺三个水平紧密联系,组成下丘脑-垂体-甲状腺轴。此外,甲状腺还可进行一定程度的自身调节。
(一)下丘脑-腺垂体对甲状腺的调节
腺垂体分泌的促甲状腺激素(thyroid stimulating hormone,TSH)是调节甲状腺功能的主要激素。TSH是一种糖原白激素,分子量为28000,由α和β两个亚单位组成,α亚单位有96个氨基酸残基,其氨基酸顺序与LH、FSH和hCG的α亚单位相似;β亚单位有110个氨基酸残基,其顺序与以上三种激素有β亚单位完全不同。TSH的生物活性主要决定于β亚单位,但水解下来的单独β来只有微弱的活性,只有α亚单位与β亚单位结合在一起共同作用,才能显出全部活性。
血清中TSH浓度为2-11mU/L,半衰期约60min。腺垂体TSHA呈脉冲式释放,每2-4h出现一次波动,在脉冲式释放的基础上,还有日周期变化,血中TSH浓度清晨高而午后低。
TSH的作用是促进甲状腺激素有合成与释放。给予TSH最早出现的效果是甲状腺球蛋白水解与T4、T3的释放。给TSH数分钟内,甲状腺腺泡上皮细胞靠吞饮把胶质小滴吞入细胞内,加速T4与T3的释放,随后增强碘的摄取和甲状腺激素的合成。TSH还能促进腺泡上皮细胞的葡萄糖氧化,尤其经已糖化旁路,可提供过氧化酶作用所需要的还能型辅酶Ⅱ(NADPH) 。TSH的长期效应是刺激甲状腺细胞增生,腺体增大,这是由于TSH刺激腺泡上皮细胞核酸与蛋白质合成增强的结果。切除垂体之后,血中TSH迅速消失,甲状腺发生萎缩,甲状腺激素分泌明显减少。
在甲状腺腺泡上皮细胞存在TSH受体,它是含有750个氨基酸残基的膜蛋白,分子量为85000。TSH与其受体结合后,通过G蛋白激活腺苷酸环化酶,使cAMP生成增多,进而促进甲状腺激素的释放与合成。TSH还可通过磷脂酰肌醇系统刺激甲状腺激素的释放与合成。
有些甲状腺功能亢进患者,血中可出现一些免疫球蛋白物质,其中之一是人类刺激甲状腺免疫球蛋白(human thyroid-stmulating immunoglobulin,HTSI),其化学结构与TSH相似,它可与TSH竞争甲状腺细胞腺上的受体刺激甲状腺,这可能是引起甲状腺功能亢进的原因之一。
腺垂体TSH分泌受下丘脑TRH的控制。下丘脑TRH神经元接受神经系统其他部位传来的信息影响,把环境因素与TRH神经元活动联系起来,然后TRH神经元释放TRH,作用于腺垂体。例如,寒冷刺激的信息到达中枢神经中枢神经系统,一方面传入下丘脑体温调节中枢,同时还与该中枢接近的TRH神经元发生联系,促进TRH释放增多,进而使腺垂体TRH分泌增加。在这一过程中,去甲上腺素趣了重要的递质作用,它能增强TRH神经元释放TRH,如阻断去甲肾上腺素的合成,则机体对寒冷刺激引起的这一适应性反应大大减弱。另外,下丘脑还可通过生长抑素减少或停止TRH的合成与释放。例如,应激刺激也可通过单胺能神经元影响生长抑素的释放,如外科手术与严重创伤将引起生长抑素的释放,从而使腺垂体分泌的TRH减少,T4与T3的分泌水平降低,减少机体的代谢消耗,有利于创伤修复过程。
(二)甲状腺激素的反馈调节
血中游离的T4与T3浓度的升降,对腺垂体TSH的分泌起着经常性反馈调节作用。当血中游离的T4与T3浓度增高时,抑制TSH分泌。实验表明,甲状腺激素抑制TSH分泌的作用,是由于甲状腺激素刺激腺垂体促甲状腺激素细胞产生一种抑制性蛋白,它使TSH的合成与释放减少,并降低腺垂体对TRH的反应性。由于这种抑制作用需要通过新的蛋白质合成,所以需要几小时后方能出现效果,而且可被放线菌D与放线菌酮所阻断。T4与T3比较,T3对腺垂体TSH分泌的抑制作用较强,血中T4与T3对腺垂体这种反馈作用与TRH的刺激作用,相互拮抗,相互影响,对腺垂体TSH的分泌起着决定性作用。
关于甲状腺激素对下丘脑是否有反馈调节作用,实验结果很不一致,尚难有定论。
另外,有引起激素也可影响腺垂体分泌TSH,如雌激素可增强腺垂体对TRH的反应,从而使TSH分泌增加,而生长素与糖皮质激素则对TSH的分泌有抑制作用。
(三)甲状腺的自身调节
除了下丘脑-垂体对甲状腺进行调节以及甲状腺激素的反馈调节外,甲状腺本身还具有适应碘的供应变化,调节自身对碘的摄取以及合成与释放甲状腺激素的能力;在缺乏TSH 或TSH浓度不变的情况下,这种调节仍能发生,称为自身调节。它是 一个有限度的缓慢的调节 系统。血碘浓度增加时,最初T4与T3的合成有所增加,但碘量超过一定限度后,T4与T3的合成在维持一高水平之后,旋即明显下降,当血碘浓度超过1mmol/L时,甲状腺摄碘能力开始下降,若血碘浓度达到10mmol/L时,甲状腺聚碘作用完全消失,即过量的碘可产生抗甲状腺效应,称为Wolff-Chaikoff效应。过量的碘抑制碘转运的机制,尚不十分清楚。如果在持续加大碘量的情况下,则抑制T4与T3合成的现象就会消失,激素的合成再次增加,出现对高碘含量的适应。相反,当血碘含量不足时,甲状腺将出现碘转运机制增强,并加强甲状腺激素的合成。
(四)自主神经对甲状腺活动的影响
荧光与电镜检查证明,交感神经直接支配甲状腺腺泡,电刺激一侧的交感神经,可使该侧甲状腺激素合成增加;相反,支配甲状腺的胆碱能纤维对甲状腺激素的分泌则是抑制性的。
甲状旁腺分泌的甲状腺激素(parathyroid hormone,PTH)与甲状腺C细胞分泌的降钙素(calcitonin,CT)以及1,25-二羟维生素D3共同调节钙磷代谢,控制血浆中钙和磷的水平。
一、甲状旁腺激素
PTH是甲状旁腺主细胞分泌的含有84个氨基酸的直链肽,分子量为9000,其生物活性决定于N端的第1-27个氨基酸残基。在甲状旁腺主细胞内先合成一个含有115个氨基酸的前甲状旁腺激素原(prepro-PTH),以后脱掉N端二十五肽,生成九十肽的甲状旁腺激素原(pro-PTH),再脱去6个氨基酸,变成PTH。
在甲状旁腺主细胞内,部分PTH分子可以第33位与第40位氨基酸残基之间裂解,形成两个片断,可与PTH一同进入血中。正常人血浆PTH 浓度为10-50ng/L,半衰期为20-30min。PTH主要在肝水解灭活,代谢产物经肾排出体外。
近年从鳞状上皮癌伴发高血钙的患者癌组织中,分离出一种在化学结构上类似PTH的肽,称为甲状旁腺激素相关(parathyroid hormone related peptide,PTHrp),并进一步发现正常组织如皮肤、乳腺以及胎儿甲状旁腺中也存在这种肽。PTHrp与PTH从来源上是同族的,尤其两者的N端1-13位氨基酸残其完全相同,PTHrp也具有PTH活性。
(一)甲状旁腺激素的生物学作用
PTH是调节血钙水平的最重要激素,它有升高血钙和降低血磷含量的作用。将动物的甲状旁腺摘除后,血钙浓度逐渐降低,而血磷含量则逐渐升高,直至动物死亡。在人类,由于外科切除甲状腺时不慎,误 将甲状旁腺摘除,可引起严重的低血钙。钙离子对维持神经和肌肉组织正常兴奋性起重要作用,血钙浓度降低时,神经和肌肉的兴奋性异常增高,可发生低血钙性手足搐搦,严重时可引起呼吸肌痉挛而造成窒息。
PTH对靶器官的作用是通过cAMP系统而实现的。
1.对骨的作用 骨是体内最大的钙贮存库,PTH动员骨钙入血,使血钙浓度升高,其作用包括快速效应与延缓效应两个时相。
(1)快速效应:在PTH作用后数分钟即可发生,是将位于骨和骨细胞之间的骨液中的钙转运至血液中,骨细胞和成骨细胞在骨内形成一个膜系统,全部覆盖了骨表面和腔隙的表面,在骨质与细胞外液之间形成一层可通透性屏障。在骨膜与骨质之间含有少量骨液,骨液中含有Ca2+(只有细胞外流人的1/3)。PTH能迅速提高骨细胞膜对Ca2+的通透性,使骨液中的钙进入细胞,进而使骨细胞膜上的钙泵活动增强,将Ca2+转运到细胞外液中。
(2)延缓效应:在PTH作用后2-14h出现,通常在几天甚至几周后达高峰,这一效应是通过刺激破骨细胞活动增强而实验的。PTH既加强已有的破骨细胞的溶骨活动,又促进破骨细胞的生成。破骨细胞向周围骨组织伸出绒毛样突起,释放蛋白水解酶与乳酸,使骨组织溶解,钙与磷大量入轿,使血钙浓度长时间升主。PTH的两个效应相互配合,不但能对血钙急切需要作出迅速应答,而且能使血钙长时间维持在一定水平。
2.对肾的作用 PTH促进远球小管对钙的重吸收,使尿钙减少,血钙升高,同时还抑制近球不管对磷的重吸收,增加尿磷酸盐的排出,使血磷降低。
此外,PTH对肾的另一重要作用是激活α-羟化酶,使25-羟维生素D3(25-OH-D3)转变为有活性的1,25-二羟维生素D3(1,25-(OH)2-D3)。
3.1,25-(OH)2-D3的生成与作用 体内的VD3(维生素D3)主要由皮肤中7-脱氢胆固醇经日光中些外线照射转化而来,也可由动物性食物中获取。VD3无生物活性,它首先需在肝羟化成25-OH-D3,然后在肾又 进一步转化成1,25-(OH)2-D3,其作用为:①促进小肠粘膜上皮细胞对钙的吸收,这是由于1,25-(OH)2-D3进入小肠粘膜细胞内,与胞浆受体结合后进入细胞核,促进转录过程,生成一咱与钙有很高亲和力的钙结合蛋白(calcium-binding protein),参与钙的转运而促进钙的吸收。PTH在增强钙的吸收的同时也促进磷的吸收;②对骨钙动员和骨盐沉积有作用,一方面促进钙、磷的吸收,增加血钙、血磷含量,刺激成骨细胞的活动,从而促进骨盐沉积和骨的形成。另一方面,当血钙浓度降低时,又能提高破骨细胞的活性,动员骨钙入血,使血钙浓度升高。另外,1,25-(OH)2-D3能增强PTH对骨的作用,在缺乏1,25-(OH)2-D3时,PTH的作用明显减弱。
(二)甲状旁腺激素分泌的调节
PTH的分泌主要受血浆钙浓度变化的调节。血浆钙浓度轻微下降时,就可使甲状旁腺分泌PTH迅速增加,血钙浓度降低可直接刺激甲状旁腺细胞释放PTH,PTH动员骨钙入轿,增强肾重吸收钙,结果使已降低了血钙浓度迅速回升。相反,血钙浓度升高时,PTH分泌减少。长时间的高血钙,可使甲状旁腺发生萎缩,而长时间的低血钙,则可使甲状旁腺增生。
PTH的分泌还受其他一些因素的影响,如血磷升高可使血钙降低而刺激PTH的分泌。血Mg2+浓度很低时,可使PTH分泌减少。另外,生长抑素也能抑制PTH的分泌。
二、降钙素
降钙素是含有一个二硫键的三十二肽,分子量为3400。正常人血清中降钙素浓度为10-20ng/L,血浆半衰期小于1h,主要在肾降解并排出,降钙素整个分子皆为激素活性所必需。
(一)降钙素的生物学作用
降钙素的主要作用是降低血钙和血磷,其主要靶器官是骨,对肾也有一定的作用。
1.对骨的作用 降钙素抑制破骨细胞活动,减弱溶骨过程,这一反应发生很快,大剂量的降钙素在15min内便可使破骨细胞活动减弱70%。在给降钙素1h左右,出现成骨细胞活动增强,持续几天之久。这样,降钙素减弱溶骨过程,增强成骨过程,使骨组织释放的钙磷减少,钙磷沉积增加,因而血钙与血磷含量下降。
成人降钙素对血钙的调节作用较小,因为降钙素引起的血钙浓度下降,可强烈地刺激PTH的。PTH的作用完全可以超过降钙素的效应。另外,成人的破骨细胞每天只能向细胞外液提供0.8g钙,因此,抑制破骨细胞的活动对血钙的影响是很小的。然而,儿童骨的更新速度很快,破骨细胞活动每天可向细胞外液提供5g以上的钙,相当于细胞外液总钙量的5-10倍,因此,降钙素对儿童血钙的调节则十分明显。
2.对肾的作用 降钙素能抑制肾小管对钙、磷、钠及氯的重吸收,使这些离子从尿中排出增多。
(二)降钙素分泌的调节
降钙素的分泌主要受血钙浓度的调节。当血钙浓度升高时,降钙素的分泌亦随之增加,降钙素与PTH对血钙的作用相反,区同调节血钙浓度的相对稳定。比较降钙素与PTH对血钙的调节作用,有两个主要的差别:①降钙素分泌启动较快,在1h内即可达到高峰,而PTH分泌则需几个小时;②降钙素只对血钙水平产生短期调节作用,其作用很快被有力的PTH作用所克服,后者对血钙浓度发挥长期调节作用,由于降钙素的作用快速而短暂,所以,对高钙饮食引起的血钙升高回复到正常水平起着重要作用。进食可刺激降钙素的分泌。这可能与几种胃肠激素如胃泌素、促胰液素以及胰高血糖素的分泌有关,它们都有促进降钙素分泌的作用,其中以胃泌素的作用最强。
肾上腺包括中央部的髓质和周围部的皮质两个部分,两者在发生、结构与功能上均不相同,实际上是两种内分泌腺。
一、肾上腺皮质
肾上腺皮质分泌的皮质激素分为三类,即盐皮质激素、糖皮质激素和性激素。各类皮质激素是由肾上腺皮质不同层上皮细胞所分泌的,球状带细胞分泌盐皮质激素,主要是醛固醇(aldosterone);束状带细胞分泌糖皮质激素,主要是皮质醇(cortisol);网状带细胞主要分泌性激素,如脱氢雄酮(dehydroepiandrosterone)和雌二醇(estradiol)也能分泌少量的糖皮质激素。肾上腺皮质激素属于类固醇(甾体)激素,其基本结构为环戊烷多氢菲。盐皮质激素与糖皮质激素是21个碳原子的类固醇,雄激素含有19个碳原子,雌激素含有18个碳原子。
胆固醇是合成肾上腺皮质激素的原料,主要来自血液。在皮质细胞的线粒体内膜或内质网中所含的裂解酶与羟化酶等酶系的作用下,使胆固醇先变成孕烯酮,然后再进一步转变为各种皮质激素。由于肾上腺皮制裁各层细胞存在的酶系不同,所以合成 皮质激素亦不相同。
皮质醇进入血液后,75%-80%与血中皮质类固醇结合球蛋白(corticosteroid-binding globulin,CBG)或称为皮质激素运载蛋白结合,15%与血浆白蛋白结合,5%-10%的皮质醇是游离的。结合型与游离型皮质醇可以相互转化,维持动态平衡。游离的皮质醇能进入靶细胞发挥其作用。CBG是肝产生的α2球蛋白,分子量为52000,血浆中CBG浓度为30-50mg/L。CBG与皮质醇有较强有亲和力,每一分子的CBG仅有一个结合位点,只能结合一个分子的皮质醇。每100ml血浆CBG能结合20μg皮质醇。可见,CBG在运载皮质醇方面起着重要作用,。醛固醇与血浆白蛋白及CBG的结合能力很弱,主要以游离状态存在和运输。
皮质醇在血浆中半衰其为70min,醛固醇为20min。它们都在肝中降解,皮质醇首先是在C4GN C5间的双键加氢还原,形成双氢皮质醇,随后,C3上的酮基变成羟基产生四氢皮质醇,与葡萄糖醛酸或硫酸结合,随尿排出体外。四氢皮质醇是皮质醇的主要代谢产物,点尿中皮质醇代谢物排出量的45%-50%。四氢皮质醇和皮五醇在C20酮基变为痉基生成皮五醇,占尿中排出量的20%左右。由于四氢皮质醇和皮五醇在C17上均有羟基,故称为17-羟类固醇。另外,C1`7上脱去侧链,生成17-氧类固醇,占尿中排出题 的10%左右。醛固醇基本上循类似途径被处理。
肾上腺皮质网状带分泌的性激素以脱氢异雄酮为主,它是一种17-氧类固醇,睾酮的代谢产物也是17-氧类固醇。因此,男子尿中17-氧类固醇的来源有睾丸分泌的睾酮和肾上腺皮质分泌的皮质醇及雄激素。
(二)肾上腺皮质激素的生物学作用
动物摘除双侧肾上腺后,如不适当处理,一二周即死去,如仅切除肾上腺髓质,动物可以存活较长时间,说明肾上腺皮质是维持生命所必需的。分析动物死亡的原因,主要有两个方面:其一是机体水盐损失严重,导致血压降低,终于因循环衰竭而死,这主要是缺乏盐皮质激素所致;其二是糖、蛋白质、脂肪等物质代谢发生严重紊乱,对各种有害刺激的抵抗力降低,导致功能活动失常,这是由于缺乏糖皮质激素的缘故。若及时补充肾上腺皮质激素,动物的生命可以维持。
1.糖皮质激素 人体血浆中糖皮质激素主要为皮质醇,其次为皮质酮,但皮质酮的含量仅为皮质醇的1/20-1/10。
(1)对物质代谢的影响:糖皮质激素对糖、蛋白质和脂肪代谢均有作用。①糖代谢;糖皮质激素是调节机体糖代谢的重要激素之一,它促进糖异生,升高血糖,这是由于它促进蛋白质分解,有较多的氨基酸进入肝,同时增强肝内与糖异生有关酶的活性,致使糖异生过程大大加强。此外,糖皮质激素又有抗胰岛素作用,促进血糖升主。如果糖皮质激素分泌过多(或服用此类激素药物过多)可引起血糖升高,甚至出现糖尿;相反,肾上腺皮质功能低下患者(如阿多数狄森病),则可出现低血糖; ②蛋白质代谢:糖皮质激素促进肝外组织,特别是肌肉组织蛋白质分解,加速氨基酸转移至肝生成肝糖原。糖皮质激素分泌过多时,由于蛋白质分解增强,合成减少,将出现肌肉消瘦、骨质疏松、皮肤变薄、淋巴组织萎缩等;③脂肪代谢:糖皮质激素促进脂肪分解,增强脂肪酸在肝内氧化过程,有利于糖异生作用。肾上腺皮质功能亢进时,糖皮质激素对身体不同部位的脂肪作用不同,四肢脂肪组织分解增强,而腹、面、肩及背有脂肪合成有所增加,以致呈现面圆、背厚、躯干部发胖而四肢消瘦的特殊体形。
(2)对水盐代谢的影响:皮质醇有较弱的贮钠排钾作用,即对肾远由小管及集合管重吸收和排出钾有轻微的促进作用。此外,皮质醇还可以降低肾小球入球血管阻力,增加肾小球血浆流量而使肾小球滤过率增加,有利于水的排出。皮质醇对水负荷时水的快速排出有一定的作用,肾上腺皮质功能不足患者,排水能力明显降低,严重时可出现“水中毒”,如补充适量的糖皮质激素即可得到缓解,而补充盐皮质激素则无效。有资料指出,在缺乏皮质醇时,ADH释放增多,集合管对水的重吸收增加。
(3)对血细胞的影响:糖皮质激素可使血中红细胞、血小板和中性粒细胞的数量增加,而使淋巴细胞和嗜酸性粒细胞减少,其原因各有不同。红细胞和血小板的增加,是由于骨髓造血功能增强;中性粒细胞的增加,可能是由于附着在小血管壁边缘的中性粒细胞进入血液循环增多所致;至于淋巴细胞减少,可能是糖皮质激素使淋巴细胞DNA合成过程减弱,抑制胸腺与淋巴组织的细胞分裂。此外,糖皮质激素还能促进淋巴细胞与渚酸性粒细胞破坏。
(4)对循环系统的影响:糖皮质激素对维持正常血压是必需的,这是由于:①糖皮质激素能增强血管平滑肌对儿茶酚胺的敏感性(允许作用),这可能由于糖皮质激素能啬血管平滑肌细胞膜上的儿茶酚胺受体数量以及调节受体介导的细胞内的信息传递过程;②糖皮质激素能抑制具有血管舒张作用的前列腺素的合成;③糖皮质激素能降低毛细血管的通透性,有利于维持血容量。肾上腺皮质功能低下时,血管平滑肌对儿茶酚胺的反应性降低,毛细血管扩张,通透性增加,血压下降,补充皮质醇后可恢复。
另外,离体实验证明,糖皮质激素可增强心肌的收缩力,但在整体条件下对心脏的作用并不明显。
(5)在应激反应中的作用:当机体受到各种有害刺激,如缺氧、创伤、手术、饥饿、疼痛、寒冷以及精神紧张和焦虑不安等。血中ACTH浓度立即增加,糖皮质激素也相应增多。能引起ACTH与糖皮质激素分泌增加的各种刺激称为应激刺激,而产生的反应称为应激(stress)。在这一反应中,除垂体-肾上腺皮质系统参加外,交感-肾上腺髓质系统也参加,所以,在应激反应中,血中儿茶酚胺含量也相应增加。切珍重肾上腺髓质的动物,可以抵抗应激而不产生严重后果,而当去掉肾上腺皮质时,则机体应激反应减弱,对有害刺激的抵抗力大大降低,严重时可危及生命。应激反应可能从以下几个方面调节机体的适应能力:
①减少应激刺激引起的一些物质(缓激肽、蛋白水解酶及前列腺素等)的产生量及其不良作用;②使能量代放运转以糖代谢为中心,保持葡萄糖对重要器官(如脑和心)的供应;③在维持血压方面起允许作用,增强儿茶酚胺对血管的调节作用。应该指出,在应激反应中,除了ACTH、糖皮质激素与儿茶酚胺的分泌增加外,β-内啡肽、生长素、催乳素、抗利尿激素、胰主血压素及醛固醇等均可增加,说明应激反应是多种激素参与并使机体抵抗力增强的非特异性反应。
糖皮质激素的作用广泛而复杂,以上仅简述了它们的主要作用。此外,还有多方面的作用,如促进胎儿肺表面活性物质的合成,增强骨骼肌的收缩力,提高胃腺细胞对迷走神经与胃泌素的反应性,增加胃酸与胃蛋白酶原的分泌,抑制骨的形成而促进其分解等。临床上使用大剂量的糖皮质激素及其类似物,可用于抗炎、抗过敏、抗毒和抗休克。
2.盐皮质激素 主要为醛固醇,对水盐代谢的作用最强,其次为脱氧皮质醇。
醛固酮是调节机体水盐代谢的重要激素,它促进肾远曲小管及集合管重吸收钠、水和排出钾,即保钠、保水和排钾作用。当醛固酮分泌过多时,将使钠和水贮留,引起高血钠、高血压和血钾降低。相反,醛固酮缺乏时则钠与水的排出过多,血钠减少,血压降低,而尿钾排出减少,血钾升高。关于醛固酮对肾的作用及其机制,可参阅第八章,另外,盐皮质激素与糖皮质激素一样,以增强血管平滑肌对儿茶酚胺的敏感性,且作用比糖皮质激素更强。
(三)肾上原皮质激素分泌的调节
1.糖皮质激素分泌的调节 肾上腺皮质分泌皮质激素的束状带及网状带,处于腺垂体保肾上腺皮质激素(adrenocortiotropin,ACTH)的经常性控制之下,无论是糖皮质激素的基础分泌,还是在应激状态下的分泌,都受ACTH的调控,切除动物的垂体后,束状带与网状带萎缩,糖皮质激素有分泌显著减少,如及时补充ACTH,可使已发生萎缩的束状带与网状带基本恢复,糖皮质激素有分泌回升。
(1)ACTH:ACTH是一个含39个氨基酸的多肽,分子量为4500。
ACTH分子上的1-24位氨基酸为生物活性所必需的,25-39位氨基酸可保护激素,减慢降解,延长作用时间。各种动物的ACTH前24位氨基酸均相同,因此,从动物(牛、羊、猪等)腺垂体提到的ACTH对人有效。目前 ,ACTH已能人工合成。在垂体,ACTH是由阿黑皮素原(POMC)经酶分散而来,同时产生β-MSH。ACTH再经酶分解生成α-MSH,ACTH的第4-10位氨基酸与α-MSH第4-10位氨基酸和β-MSH第11-17位氨基酸相同,这部分氨基酸是产生MSH活性最小单位,因此ACTH也具有促黑素细胞 产生黑色素的作用。
ACTH的分泌呈现日节律波动,入睡后ACTH分泌逐渐减少,午夜最低,随后又逐渐增多,至觉醒起床前进入分泌高峰,白天维持在较低水平,入睡时再减少。由于ACTH分泌的日节律波动,促糖皮质激素的分泌也出现相应的波动。ACTH分泌的这种日节律波动,是由下丘脑CRH节律性释放所决定的。
ACTH 不但刺激糖皮质激素的分泌,也刺激束状带与网状带细胞的生长发育,关于ACTH的作用机制已基本清楚。在束状还与网状带细胞膜上存在ACTH特异性受体,在Ca2+存在的条件下,ACTH与膜受体结合,激活腺苷酸环化酶,通过cAMP激活蛋白激酶,蛋白激酶起三项重要作用;①使核糖蛋白磷酸化,促进mRNA形成一种特殊蛋白质,使胆固醇得以进入线粒体,并经侧链解形成孕烯醇酮,以进一步合成糖皮质激素;②使磷酸化酶活化,促进糖原分解,产生ATP,提供能量,另外还通过戊糖旁路产生还原型辅酶Ⅱ(NADPH),以利胆固醇的羟化过程;③使胆固醇酯活化,促进其转变为胆固醇,提供激素合成的原料。在ACTH促进肾上腺皮质细胞合成糖皮质激素的同时,束状带细胞膜对葡萄糖与胆固醇的转运机制增强,使 较多的葡萄糖与胆固醇进入细胞内。
(2)ACTH分泌的调节:ACTH调节糖皮质激素的分泌,而ACTH的分泌受下丘脑CRH的控制又与糖皮质激素有反馈调节。下丘脑CRH神经元和其他下丘脑调节肽神经元一样,又受脑内神经递质的调控。应激刺激作用于神经系统的不同部位,最后通过神经递质,将信息汇集于CRH神经元,然后借CRH控制腺垂体的促肾上腺皮质激素细胞分泌ACTH。此外,当血中糖皮质激素浓度升高时,可使腺垂体释放ACTH减少,ACTH的合成也受到抑制,腺垂体对CRH的反应也性减弱。糖皮质激素的负反馈调节主要作用于垂体,也可作用于下丘脑,这后一种反馈称为长反馈。ACTH还可反馈抑制CRH神经元,称为短反馈。至于是否存在CRH对CRH神经地的超短反馈,尚不能肯定。
综上所述,下丘脑、垂体和肾上腺皮质组成一个密切联系、协调统一的功能活动轴,从而维持血中糖皮质激素浓度的相对稳定和在不同状态下的适应性变化。
2.盐皮质激素分泌的调节 醛固酮的分泌主要受肾素-血管紧张素系统的调节。另外,血K+,血Na+浓度可以直接作用于球状带,影响醛固酮的分泌。
在正常情况下,ACTH对醛固酮的分泌并无调节作用,但切除垂体后,在应激醛固酮的分泌反应减弱,提示在应激情况下,ACTH对醛固酮的分泌可能起到一定的支持作用。
二、肾上腺髓质
肾上腺髓质嗜铬细胞分泌肾上腺素(epinephrine,E)和去甲肾上腺素(norepinephrine,NE)都是儿茶酚胺激素。
(一)髓质激素的合成与代谢
髓质激素的合成与交感神经节后纤维合成去甲肾上腺素的过程基本一致,不同的是在嗜铬细胞胞浆中存在大量的苯乙醇胺氮位甲基移位酶(phenylethanolamine-N-methyltransferase,PNMT),可使去甲肾上腺素甲基化而成肾上腺素。合成髓质激素有原料分为酪氨酸,其合成过程为:酪氨酸→多巴→多巴胺→去甲肾上腺素→肾上腺素,各个步骤分别在特异酶,如酷氨酸羟化酶、多巴脱羟酶、多巴胺β-羟化酶及PNMT的作用下,最后生成肾上腺素。
肾上腺素与去甲肾上腺素一起贮存在髓质细胞的囊泡里内,以待释放。髓质中肾上腺素与去甲肾上腺素的比例大约为4:1,以肾上腺素为主。在血液中去甲肾上腺素除由髓质分泌外,主要来自肾上腺素能神经纤维末梢,而血中肾上腺素主要来自肾上腺髓质。
在体内的肾上腺素与去甲肾上腺素通过单胺氧化酶(monoamine oxidase,MAO)与儿茶酚-O-甲基移位酶(catechol-O-methyltransferase,COMT)的作用而灭活。
(二)髓质激素的生物学作用
髓质与交感神经系统组成交感-肾上腺髓质系统,或称交感-肾上腺系统,所以,髓质激素的作用与交感神经紧密联系,难以分开 。生理学家Cannon最早全面研究了交感-肾上腺髓质系统的作用,曾提出应急学说(emergency reaction hypothesis),认为机体遭遇特殊情况时,包括畏惧、剧痛、失血、脱水、乏氧、暴冷暴热以及剧烈运动等,这一系统将立即调动起来,儿茶酚胺(去肾上腺素、肾上腺素)的分泌量大大增加。儿茶酚胺作用于中枢神经系统,提高其兴奋性,使机体处于警觉状态,反应灵敏;呼吸加强加快,肺通气量增加;心跳加快,心缩力增强,心输出量增加。血压升高,血液循环加快,内脏血管收缩,骨骼肌血管舒张同时血流量增多,全身血液重新分配,以利于 应急时重要器官得到更多的血液供应;肝糖原分解增加,血糖升高,脂肪分解加强,血中游离脂肪酸增多,葡萄糖与脂肪酸氧化过程增强,以适应在应急情况下对能量的需要。总之,上述一切变化都是在紧急情况下,通过交感-肾上腺髓质系统发生的适应性反应,称之为应急反应。实际上,引起应急反应的各种刺激,也是引起应激反应的刺激,当机体受到应激刺激时,同时引起应急反应与应激反应,两者相辅相成,共同维持机体的适应能力。
(三)髓质激素分泌的调节
1.交感神经 髓质受交感神经胆碱能节前纤维支配,交感神经兴奋时,节前纤维末梢释放乙酰胆碱,作用于髓质嗜铬细胞上的N型受体,引起肾上腺素与去甲肾上腺素的释放。若交感神经兴奋时间较长,则合成儿茶酚胺所需要的酪氨酸羟化酶、多巴胺β-羟化酶以及PNMT的活性均增强,从而促进儿茶酚胺的合成。
2.ACTH与糖皮质激素 动物摘除垂体后,髓质中酪氨酸氢化酶、多巴胺β-羟化酶与PNMT的活性降低,而补充ACTH则能使这种酶的活性恢复,如给予糖皮质激素可使多巴胺β-羟化酶与PNMT活性恢复,而对酪酸羟化酶未见明显影响,提示ACTH促进髓质合成儿茶酚胺的作用,主要通过糖皮质激素,也可能有直接作用。肾上腺皮质的血液经髓质后才流回循环,这一解剖特点有利于糖皮质激素直接进入髓质,调节儿茶酚胺的合成。
3.自身反馈调节 去甲肾上腺素或多巴胺在髓质细胞内的量增加到一定数量时,可抑制酪氨酸羟化酶。同样,肾上腺素合成增多时,也能抑制PNMT的作用,当肾上腺素与去甲肾上腺素从细胞内释入血液后,胞浆内含量减少,解除了上述的负反馈抑制,儿茶酚胺的合成随即增加。
人类的胰岛细胞按其染色和形态学特点,主要分为A细胞、B细胞、D细胞及PP细胞。A细胞约占胰胰岛细胞的20%,分泌胰主血糖素(glucagon);B细胞占胰岛细胞的60%-70%,分泌胰岛素(insulin);D细胞占胰岛细胞的10%,分泌生成抑素;PP细胞数量很少,分泌胰多肽(pancreatic polyeptide)。
一、胰岛素
胰岛素是含有51个氨基酸的小分子蛋白质,分子量为6000,胰岛素分子有靠两个二硫键结合的A链(21个氨基酸)与B链(30个氨基酸),如果二硫键被打开则失去活性。B细胞先合成一个大分子的前胰岛素原,以后加工成八十六肽的胰岛素原,再经水解成为胰岛素与连接肽(C肽)。
胰岛素与C肽共同释入血中,也有少量的胰岛素原进入血液,但其生物活性只有胰岛素的3%-5%,而C肽无胰岛素活性。由于C肽是在胰岛素合成过程产生的,其数量与胰岛素的分泌量有平行关系,因此测定血中C肽含量可反映B细胞的分泌功能。正常人空腹状态下血清胰岛素浓度为35-145pmol/L。胰岛素在血中的半衰期只有5min,主要在肝灭活,肌肉与肾等组织也能使胰岛素失活。
1965年,我国生化学家首先人工合成了具有高度生物活性的胰岛素,成为人类历史上第一次人工合成生命物质(蛋白质)的创举。
(一)胰岛素的生物学作用
胰岛素是促进合成代谢、调节血糖稳定的主要激素。
1.对糖代谢的调节 胰岛素促进组织、细胞对葡萄糖的摄取和利用,加速葡萄糖合成为糖原,贮存于肝和肌肉中,并抑制糖异生,促进葡萄糖转变为脂肪酸,贮存于脂肪组织,导致血糖水平下降。
胰岛素缺乏时,血糖浓度升高,如超过肾糖阈,尿中将出现糖,引起糖尿病。
2.对脂肪代谢的调节 胰岛素促进肝合成脂肪酸,然后转运到脂肪细胞贮存。在胰岛素的作用下,脂肪细胞也能合成少量的脂肪酸。胰岛素还促进葡萄糖进入脂肪细胞,除了用于合成脂肪酸外,还可转化为α-磷酸甘油,脂肪酸与α-磷酸甘油形成甘油三酯,贮存于脂肪细胞中,同时,胰岛素还抑制脂肪酶的活性,减少脂肪的分解。
胰岛素缺乏时,出现脂肪代谢紊乱,脂肪分解增强,血脂升高,加速脂肪酸在肝内氧化,生成大量酮体,由于糖氧化过程发和障碍,不能很好处理酮体,以致引起酮血症与酸中毒。
3.对蛋白质代谢的调节 胰岛素促进蛋白质合成过程,其作用可在蛋白质合成的各个环节上:①促进氨基酸通过膜的转运进入细胞;②可使细胞核的复制和转录过程加快,增加DNA和RNA的生成;③作用于核糖体,加速翻译过程,促进蛋白质合成;另外,胰岛素还可抑制蛋白质分解和肝糖异生。
由于胰岛素能增强蛋白质的合成过程,所以,它对机体的生长也有促进作用,但胰岛素单独作用时,对生长的促进作用并不很强,只有与生长素共同作用时,才能发挥明显的效应。
近年的研究表明,几乎体内所有细胞的膜上都有胰岛素受体。胰岛素受体已纯化成功,并阐明了其化学结构。胰岛素受体是由两个α亚单位和两个β亚单位构成的四聚体,α亚单位由719个氨基酸组成,完全裸露在细胞膜外,是受体结合胰岛素的主要部位。α与α亚单位、α与β亚单位之间靠二硫键结合。β亚单位由620个氨基酸残基组成,分为三个结构域:N端194个氨基酸残基伸出膜外;中间是含有23个氨基酸残基的跨膜结构域;C端伸向膜内侧为蛋白激酶结构域。胰岛素受体本身具有酪氨酸蛋白激酶活性,胰岛素与受体结合可激活该酶,使受体内的酪氨酸残基发生磷酸化,这对跨膜信息传递、调节细胞的功能起着十分重要的作用。关于胰岛素与受体结合启动的一系列反应,相当复杂,尚不十分清楚。
(二)胰岛素分泌的调节
1.血糖的作用 血糖浓度是调节胰岛素分泌的最重要因素,当血糖浓度升高时,胰岛素分泌明显增加,从而促进血糖降低。当血糖浓度下降至正常水平时,胰岛素分泌也迅速恢复到基础水平。在持续高血糖的刺激下,胰岛素的分泌可分为三个阶段:血糖升高5min内,胰岛素的分泌可增加约10倍,主要来源于B细胞贮存的激素释放,因此持续时间不长,5-10min后胰岛素的分泌便 下降50%;血糖升高15min后,出现胰岛素分泌的第二次增多,在2-3h达高峰,并持续较长的时间,分泌速率也远大于第一相,这主要是激活了B细胞胰岛素合成酶系,促进了合成与释放;倘若高血糖持续一周左右,胰岛素的分泌可进一步增加,这是由于长时间的高血糖刺激B细胞增生布引起的。
2.氨基酸和脂肪酸的作用 许多氨基酸都有刺激胰岛素分泌的作用,其中以精氨酸和赖氨酸的作用最强。在血糖浓度正常时,血中氨基酸含量增加,只能对胰岛素的分泌有轻微的刺激作用,但如果在血糖升高的情况下,过量的氨基酸则可使血糖引起的胰岛素分泌加倍增多。务右脂肪酸和酮体大量增加时,也可促进胰岛素分泌。
3.激素的作用 影响胰岛素分泌的激素主要有:①胃肠激素,如胃泌素、促胰液素、胆囊收缩素和抑胃肽都有促胰岛素分泌的作用,但前三者是在药理剂量时才有促胰岛素分泌作用,不像是一引起生理刺激物,只有抑胃肽(GIP)或称依赖葡萄糖的促胰岛素多肽(glucose-dependent insulin-stimulating polypeptide)才可能对胰岛素的分泌起调节作用。GIP是由十二指肠和空肠粘膜分泌的,由43个氨基酸组成的直链多肽。实验证明,GIP刺激胰岛素分泌的作用具有依赖葡萄糖的特性。口服葡萄糖引起的高血糖和GIP的分泌是平行的 ,这种平行关系的绘双导致胰岛素的迅速而明显的分泌,超过了静脉注射葡萄糖所引起的胰岛素分泌反应,。有人给大鼠口吸取葡萄糖并注射GIP抗血清,结果使血中葡萄浓度升高,而胰岛素水平却没有明显升高,因此可以认为,在肠内吸收葡萄糖期间,GIP是小肠粘膜分泌的一种主要的肠促胰岛素因子。除了葡萄糖外,小肠吸收氨基酸、脂肪酸及盐酸等也能刺激GIP的释放。有人将胃肠激素与胰岛素分泌之间的关系称为“肠-胰岛轴”,这一调节作用具有重要的生理意义,使食物尚在肠道中时,胰岛素的分泌便已增多,为即将从小肠吸收的糖、氨基酸和脂肪酸的利用做好准备;②生长素、皮质醇、甲状腺激素以及胰高血糖素告示可通过升高血糖浓度而间接刺激胰岛素分泌,因此长期大剂量应用这些激素,有可能使B细胞衰竭而导致糖尿病;③胰岛D细胞分泌的生长抑至少可通过旁分泌作用,抑制胰岛素和胰高血糖的分泌,而胰高血糖素也可直接刺激B细胞分泌胰岛素。
4.神经调节 胰岛受迷走神经与交感神经支配。刺激迷起神经,可通过乙酰胆碱作用于M受体,直接促进胰岛素的分泌;迷走神经还可通过刺激胃肠激素的释放,间接促进胰岛素的分泌。交感神经兴奋时,则通过去甲肾上腺素作用于α2受体,抑制胰岛素的分泌。
二、胰高血糖素
人胰高血糖是由29个氨基酸组成的直链多肽,分子量为3485,它也是由一个大分子的前体裂解而来。胰高血糖在血清中的浓度为50-100ng/L,在血浆中的半衰期为5-10min, 主要在肝灭活,肾也有降解作用。
(一)胰高血糖的主要作用
与胰岛素的作用相反,胰高血糖素是一种促进分解代谢的激素。胰高血糖素具有很强的促进糖原分解和糖异生作用,使血糖明显升高,1mol/L的激素可使3×106mol/L的葡萄糖迅速从糖原分解出来。胰高血糖素通过cAMP-PK系统,激活肝细胞的磷酸化酶,加速糖原分解。糖异生增强是因为激素加速氨基酸进入肝细胞,并激活糖异生过程有关的酶系。胰高血糖素还可激活脂肪酶,促进脂肪分解,同时又能加强脂肪酸氧化,使酮体生成增多。胰高血糖素产生上述代谢效应的靶器官是肝,切除肝或阻断肝血流,这些作用便消失。
另外,胰高血糖素可促进胰岛素和胰岛生长抑素的分泌。药理剂量的胰高血糖素可使心肌细胞内cAMP 含量增加,心肌收缩增强。
(二)胰高血糖素分泌的调节
影响胰高血糖素分泌的因素很多,血糖浓度是重要的因素。血糖降低时,胰高血糖素胰分泌增加;血糖升高时,则胰高血糖素分泌减少。氨基酸的作用与葡萄糖相反,能促进胰高血糖素的分泌。蛋白餐或静脉注入各种氨基酸均可使胰高血糖素分泌增多。血中氨基酸增多一方面促进胰岛素释放,可使血糖降低,另一方面还能同时刺激胰高血糖素分泌,这对防止低血糖有一定的生理意义。
胰岛素可通过降低血糖间接刺激胰高血糖素的分泌,但B细胞分泌的胰岛不比和D细胞分泌的生长抑素可直接作用于邻近的A细胞,抑制胰高血糖素的分泌(图11-22)。
胰岛素与胰高血糖素是一对作用相反的激素,它们都与血糖水平之间构成负反馈调节环路。因此,当机体外于不同的功能状态时,血中胰岛素与胰高血糖素的摩尔比值(I/G)也是不同的。一般在隔夜空腹条件下,I/G比值为2.3,但当饥饿或长时间运动时,比例可降至0.5以下。比例变小是由于胰岛素分泌减少与胰高血糖素分泌增多所致,这有利于糖原分解和糖异生,维持血糖水平,适应心、脑对葡萄糖的需要,并有利于脂肪分解,增强脂肪酸氧化供能。相反,在摄食或糖负荷后,比值可升至10以上,这是由于胰岛素分泌增加而胰高血糖素分泌减少所致。在这种情况下,胰岛不比的作用占优势。
松果体细胞是由神经细胞演变而来的,它分泌的激素主要有褪黑素和肽类激素。来自颈上交感神经节后神经末梢与松果体细胞形成突触联系,通过释放去甲上腺素控制松果体细胞的活动。
(一)褪黑素
1959年Lerner从牛松果体提取物中分离出一种能使青蛙皮肤褪色的物质,并命名为褪色素(melatonin),其化学结构为5-甲氧基-N-乙酰色胺。在松果体内羟化酶、脱羟酶、乙酰移位酶及甲基移位酶的作用下,色氨酸转变为褪色素。
松果体褪色素的分泌出现在明显的昼夜节律变化,白天分泌减少,而黑夜分泌增加。实验证明,大鼠在持续光照下,松果体重量变轻,细胞变小,合成褪色素的酶系活性明显降低,因而褪色素合成减少。反之,致盲大鼠或大鼠持续在黑暗环境中,将使松果体合成褪色素的酶系活发生 增强,褪色素的合成随之增加。摘除动物的眼球或切断支配松果体的交感神经,则褪色素分泌的昼夜节律不再出现,说明光-暗对松果体活动的影响与视觉和交感神经有关。刺激交感神经可使松果体活动增强,而β-肾上腺素能受体阻断剂可阻断交感神经对松果体的刺激作用。如毁损视交叉上核,褪色素的昼夜节律性分泌消失。所以视交叉上核被认为是控制褪色素分泌的昼夜节律中枢,在黑暗条件下,视交叉上核即发出冲动传到颈上交感神经节,其节后纤维末梢释放去甲肾上腺素,与松果体细胞膜上的β-肾上腺素能受体结合,激活腺苷酸环化酶,通过cAMP-PK系统,增强褪色素合成酶系的活性,从而导致褪色素合成增加,在光刺激下,视网膜的传入冲动可抑制交感神经的活动,使褪色素合成减少。
褪色素对下丘脑-垂体-性腺轴与下丘脑-垂体-甲状腺活动均有抑制作用。切除幼年动物的松果体,出现性早熟,性腺与甲状腺的重量增加,功能活动增强。远在一个世纪之前,人们就发出某些性早熟男孩是因松果体肿瘤所致,因此认为松果体在青春期有抗性腺功能作用。正常妇女血中褪色素在有经周期的排卵前夕最低,随后在黄体期逐渐升高,月经来潮时达到顶峰,提示妇女朋经周期的节律与松果体的节律关系密切。
(二)肽类激素
松果体能合成GnRH、TRH及8精-(氨酸)催产素等肽类激素。在多种哺乳动物(鼠、牛、羊、猪等)的松果体内GnRH比同种动物下丘脑所含的GnRH量高4-10倍。有人认为,松果体是GnRH和TRH的补充来源。
胸腺能分泌多种肽类物质,如胸腺素(thymosin)、胸腺生长素(thymopoietin)等,它们促进T细胞分化成熟。胸腺(thymus)为机体的重要淋巴器官。其功能与免疫紧密相关,分泌胸腺激素及激素类物质,具内分泌机能的器官。位于胸腔前纵隔。胚胎后期及初生时,人胸腺约重10~15克,是一生中重量相对最大的时期。随年龄增长,胸腺继续发育,到青春期约30~40克。此后胸腺逐渐退化,淋巴细胞减少,脂肪组织增多,至老年仅15克。
胸腺位于胸骨后面,紧靠心脏,呈灰赤色,扁平椭圆形,分左、右两叶,由淋巴组织构成。青春期前发充良好,青春期后逐渐退化,为脂肪组织所代替。
胸腺是造血器官,能产生淋巴细胞,并运送到淋巴结和脾脏等处。这种淋巴细胞对机体的细胞免疫具有重要作用。生长激素和甲状腺素能刺激胸腺生长,而性激素则促使胸腺退化。
胸腺的结构 表面有结缔组织被膜,结缔组织伸入胸腺实质把胸腺分成许多不完全分隔的小叶。小叶周边为皮质,深部为髓质。皮质不完全包围髓质,相邻小叶髓质彼此衔接。皮质主要由淋巴细胞和上皮性网状细胞构成,胞质中有颗粒及泡状结构。网状细胞间有密集的淋巴细胞。胸腺的淋巴细胞又称为胸腺细胞,在皮质浅层细胞较大,为较原始的淋巴细胞。中层为中等大小的淋巴细胞,深层为小淋巴细胞。从浅层到深层为造血干细胞增殖分化为小淋巴细胞的过程。皮质内还有巨噬细胞,无淋巴小结。髓质中淋巴细胞少而稀疏,上皮性网状细胞多而显著。形态多样,胞质中有颗粒及泡状结构,为其分泌物。尚有散在的圆形的胸腺小体。作用不清。
胸腺的功能有:
产生T淋巴细胞 造血干细胞经血流迁入胸腺后,先在皮质增殖分化成淋巴细胞。其中大部分淋巴细胞死亡,小部分继续发育进入髓质,成为近于成熟的T淋巴细胞。这些细胞穿过毛细血管后微静脉的管壁,循血流,再迁移到周围淋巴结的弥散淋巴组织中,此处称为胸腺依赖区。整个淋巴器官的发育和机体免疫力都必需有T淋巴细胞,胸腺为周围淋巴器官正常发育和机体免疫所必需。当T淋巴细胞充分发育,迁移到周围淋巴器官后,胸腺重要性逐渐减低。
产生和分泌胸腺素和激素类物质 从40年代开始,已从胸腺中提出十几种有效的体液因素,它们无种属特异性,在某种程度上代替胸腺机能,以微量存在于血中,以环核苷酸(cAMP)作为第二信使,可视为胸腺激素(thymin)。其中研究最多的是胸腺素(thy-mosin)。胸腺素为怀特(White)和戈尔茨坦(Goldstein)从小牛胸腺中提取出来的、分子量为12000道尔顿的蛋白质。能使免疫缺陷病人的T细胞机能得到恢复,可诱导无胸腺及去胸腺小鼠的T细胞机能,并可增加小鼠胸腺细胞中的环鸟苷酸。此外,胸腺激素Ⅰ,也是从小牛胸腺中提取出来的多肽,以后进一步提纯成胸腺激素Ⅱ,亦有诱导T细胞的机能。此激素存在于胸腺皮质或髓质上皮细胞中,而不存在胸腺细胞中。
前列腺素(prostaglandin,PG)是广泛存在于动物和人体内的一组重要的组织激素。PG的化学结构一般是具有五元环和两条侧链的二十碳不饱和脂肪酸。根据其分子结构的不同,可把PG分为A、B、D、E、F、H、I等型。
细胞膜的磷脂化在磷脂酶A2的作用下,生成PG的前体棗花生四烯酸。花生四烯酸在环氧化酶的催化下,形成不稳定的环内过氧化物棗PGG2,随后又转变为PGH2。PGH2在异构酶或还原酶的作用下,分别形成PGE2或PGF2α。PGG2与PGH2又可前列素合成酶的作用下,转变为前列环素(PGI2),在血栓烷合成酶的作用下变成血栓烷A2(TXA2)
另外,花生四烯酸在脂氧化酶的作用下,形成5-氢过氧酸,进而被代谢生成白三烯。
PG在体内代谢极快,除PGI2外,经过肺和肝被迅速降解灭活,在血浆中的半衰期公为1-2min。一般认为,PG不属于循环激素,而是在组织局部产生和释放,并对局部功能进行调节的组织激素。
PG的生物学作用极为广泛而复杂,几乎对机体各个系统的功能活动均有影响。例如,由血小板产生的TXA2,能使血小板聚集,还有能使血管收缩的作用。相反,由血管内膜产生PHG2,能抑制血小板聚集,并有舒张血管的作用。PGE2有明显的抑制胃酸分泌的作用,它可能是胃液分泌的负反馈抑制物,PGE2可增加肾血流量,促进排钠利尿。此外,PG对体温调节、神经系统、以及内分泌与生殖均有影响。
→如果您认为本词条还有待完善,请 编辑词条
上一篇神经系统(nervous system) 下一篇睾丸
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
0